15.已知下列两个热化学方程式:
H2 (g)+$\frac{1}{2}$O2(g)═H2O (l) H=-285.8kJ•mol
C3H8(g)+5O2(g)═3CO2(g)+4H2O (l) H=-2220.0kJ•mol
实验测得氢气和丙烷的混合气体共5mol,完全燃烧时放热3847kJ,则混合气体中氢气和丙烷的体积比是( )
H2 (g)+$\frac{1}{2}$O2(g)═H2O (l) H=-285.8kJ•mol
C3H8(g)+5O2(g)═3CO2(g)+4H2O (l) H=-2220.0kJ•mol
实验测得氢气和丙烷的混合气体共5mol,完全燃烧时放热3847kJ,则混合气体中氢气和丙烷的体积比是( )
| A. | 1:3 | B. | 3:1 | C. | 1:4 | D. | 5:13 |
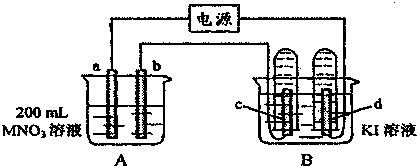
12. 如图两个装置中,液体体积均为200mL,开始工作前电解质溶液的浓度均为0.5mol/L,工作一段时间后,测得有0.02mol电子通过,若忽略溶液体积的变化,下列叙述正确的是( )
如图两个装置中,液体体积均为200mL,开始工作前电解质溶液的浓度均为0.5mol/L,工作一段时间后,测得有0.02mol电子通过,若忽略溶液体积的变化,下列叙述正确的是( )
 如图两个装置中,液体体积均为200mL,开始工作前电解质溶液的浓度均为0.5mol/L,工作一段时间后,测得有0.02mol电子通过,若忽略溶液体积的变化,下列叙述正确的是( )
如图两个装置中,液体体积均为200mL,开始工作前电解质溶液的浓度均为0.5mol/L,工作一段时间后,测得有0.02mol电子通过,若忽略溶液体积的变化,下列叙述正确的是( )| A. | 产生气体体积 ①=② | |
| B. | ①中阴极质量增加,②中正极质量减小 | |
| C. | 溶液的H+浓度变化:①增大,②减小 | |
| D. | 电极反应式①中阳极:4OH--4e-═2H2O+O2↑,②中负极:2H++2e-═H2↑ |
11.高效能电池的研发制约电动汽车的推广.有一种新型的燃料电池,它以多孔镍板为电极插入KOH溶液中,然后分别向两极通入乙烷和氧气,其总反应式为:2C2H6+7O2+8KOH═4K2CO3+10H2O,有关此电池的推断正确的是( )
| A. | 负极反应为:14H2O+7O2+28e-═28OH- | |
| B. | 放电过程中KOH的物质的量浓度不变 | |
| C. | 每消耗1 mol C2H6,则电路上转移的电子为14 mol | |
| D. | 放电一段时间后,负极周围的碱性增强 |
10. 在固态金属氧化物电解池中,高温共电解H2O-CO2混合气体制备H2和CO是一种新的能源利用方式,基本原理如图所示.下列说法不正确的是( )
在固态金属氧化物电解池中,高温共电解H2O-CO2混合气体制备H2和CO是一种新的能源利用方式,基本原理如图所示.下列说法不正确的是( )
0 172169 172177 172183 172187 172193 172195 172199 172205 172207 172213 172219 172223 172225 172229 172235 172237 172243 172247 172249 172253 172255 172259 172261 172263 172264 172265 172267 172268 172269 172271 172273 172277 172279 172283 172285 172289 172295 172297 172303 172307 172309 172313 172319 172325 172327 172333 172337 172339 172345 172349 172355 172363 203614
 在固态金属氧化物电解池中,高温共电解H2O-CO2混合气体制备H2和CO是一种新的能源利用方式,基本原理如图所示.下列说法不正确的是( )
在固态金属氧化物电解池中,高温共电解H2O-CO2混合气体制备H2和CO是一种新的能源利用方式,基本原理如图所示.下列说法不正确的是( )| A. | X是电源的负极 | |
| B. | 阴极的反应式是:H2O+2eˉ═H2+O2ˉCO2+2eˉ═CO+O2ˉ | |
| C. | 总反应可表示为:H2O+CO2═H2+CO+O2 | |
| D. | 阴、阳两极生成的气体的物质的量之比是1:1 |
 如图所示,U形管内盛有100mL的溶液,按要求回答下列问题:
如图所示,U形管内盛有100mL的溶液,按要求回答下列问题: