7.乙醚极易挥发、微溶于水、是良好的有机溶剂.乙醇与浓硫酸的混合物在不同温度下反应能生成乙烯或乙醚.某实验小组用下图装置制取乙醚和乙烯.

有关物质沸点数据
(1)制乙醚:在蒸馏烧瓶中先加入10mL乙醇,慢慢加入10mL浓硫酸,冷却,固定装置.加热到140℃时,打开分液漏斗活塞,继续滴加10mL乙醇,并保持140℃,此时烧瓶c中收集到无色液体.
①Ⅰ和Ⅱ是反应发生装置,应该选择Ⅰ(选答“Ⅰ”或“Ⅱ”)与装置Ⅲ相连.
②乙醇通过分液漏斗下端连接的长导管插入到液面下加入,目的有二,一是使反应物充分混合,二是防止乙醇挥发.
③Ⅲ中水冷凝管的进水口是b(选答“a”或“b”).冰盐水的作用是凝液化乙醚.
④有同学认为以上装置还不够完善,一是溴水可能倒吸,二是尾气弥漫在空气中遇明火危险.该同学设计了以下几种装置与导管d连接,你认为合理的是(选填编号)c、d.
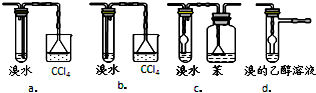
⑤反应一段时间后,升温到170℃,观察到反应物变为黑色,溴水褪色.写出实验过程中有气体生成的化学方程式(写两个方程式)CH3CH2OH+6H2SO4$\stackrel{△}{→}$2CO2↑+6SO2↑+↑+2H2O;C+2H2SO4$\stackrel{△}{→}$CO2↑+2SO2↑+2H2O、CH3CH2OH$→_{170℃}^{浓硫酸}$C2H4↑+H2O、CH3CH2OH+2H2SO4$\stackrel{△}{→}$2C+2SO2↑+5H2O(其中两个).
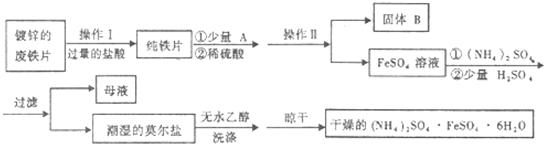
⑥实验中收集到的乙醚产品中可能含有多种杂质.某同学设计了以下提纯方案:
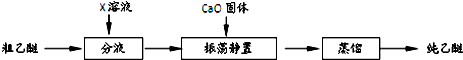
(2)分液步骤除去产品中的酸性杂质,则X可以是NaOH.
(3)蒸馏操作可除去的杂质是乙醇(CH3CH2OH).

有关物质沸点数据
| 物质 | 沸点 |
| 乙醚 | 34.6℃ |
| 乙醇 | 78.2℃ |
①Ⅰ和Ⅱ是反应发生装置,应该选择Ⅰ(选答“Ⅰ”或“Ⅱ”)与装置Ⅲ相连.
②乙醇通过分液漏斗下端连接的长导管插入到液面下加入,目的有二,一是使反应物充分混合,二是防止乙醇挥发.
③Ⅲ中水冷凝管的进水口是b(选答“a”或“b”).冰盐水的作用是凝液化乙醚.
④有同学认为以上装置还不够完善,一是溴水可能倒吸,二是尾气弥漫在空气中遇明火危险.该同学设计了以下几种装置与导管d连接,你认为合理的是(选填编号)c、d.

⑤反应一段时间后,升温到170℃,观察到反应物变为黑色,溴水褪色.写出实验过程中有气体生成的化学方程式(写两个方程式)CH3CH2OH+6H2SO4$\stackrel{△}{→}$2CO2↑+6SO2↑+↑+2H2O;C+2H2SO4$\stackrel{△}{→}$CO2↑+2SO2↑+2H2O、CH3CH2OH$→_{170℃}^{浓硫酸}$C2H4↑+H2O、CH3CH2OH+2H2SO4$\stackrel{△}{→}$2C+2SO2↑+5H2O(其中两个).
⑥实验中收集到的乙醚产品中可能含有多种杂质.某同学设计了以下提纯方案:

(2)分液步骤除去产品中的酸性杂质,则X可以是NaOH.
(3)蒸馏操作可除去的杂质是乙醇(CH3CH2OH).
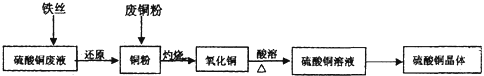
6.碘酸钾是一种白色结晶,无臭无味,酸性条件下碘酸钾是一种较强的氧化剂,与氢碘酸、二氧化硫等还原性物质作用,被还原为单质碘;在碱性介质中,碘酸钾能被氯气、次氯酸盐等氧化为高碘酸钾.碘酸钾在常温下稳定,加热至560℃开始分解.工业生产碘酸钾的流程如图,在反应器中发生反应的化学方程式为:6I2+11KClO3+3H2O═6KH(IO3)2+5KCl+3Cl2.
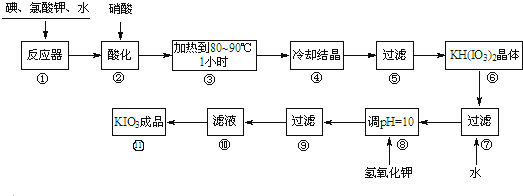
试回答下列问题:
(1)步骤①反应器发生的反应中,转移电子总数为60e-;
(2)步骤②中,用硝酸而不用HI,其原因可能是HI具有还原性,能将已生成的碘酸氢钾还原;
(3)步骤③要保持溶液微沸1小时以完全排出氯气,排出氯气的原因为Cl2及Cl2与KOH反应生成的KClO,能将KIO3氧化成KIO4;
(4)实验中涉及两次过滤,在实验室进行过滤实验中,用到的玻璃仪器有漏斗、烧杯、玻璃;
(5)步骤⑧用氢氧化钾调节溶液的pH,反应的化学方程式为:KOH+KH(IO3)2=2KIO3+H2O;
(6)参照下表碘酸钾的溶解度,步骤 得到碘酸钾晶体,你建议的方法是蒸发结晶.
得到碘酸钾晶体,你建议的方法是蒸发结晶.
0 171870 171878 171884 171888 171894 171896 171900 171906 171908 171914 171920 171924 171926 171930 171936 171938 171944 171948 171950 171954 171956 171960 171962 171964 171965 171966 171968 171969 171970 171972 171974 171978 171980 171984 171986 171990 171996 171998 172004 172008 172010 172014 172020 172026 172028 172034 172038 172040 172046 172050 172056 172064 203614

试回答下列问题:
(1)步骤①反应器发生的反应中,转移电子总数为60e-;
(2)步骤②中,用硝酸而不用HI,其原因可能是HI具有还原性,能将已生成的碘酸氢钾还原;
(3)步骤③要保持溶液微沸1小时以完全排出氯气,排出氯气的原因为Cl2及Cl2与KOH反应生成的KClO,能将KIO3氧化成KIO4;
(4)实验中涉及两次过滤,在实验室进行过滤实验中,用到的玻璃仪器有漏斗、烧杯、玻璃;
(5)步骤⑧用氢氧化钾调节溶液的pH,反应的化学方程式为:KOH+KH(IO3)2=2KIO3+H2O;
(6)参照下表碘酸钾的溶解度,步骤
 得到碘酸钾晶体,你建议的方法是蒸发结晶.
得到碘酸钾晶体,你建议的方法是蒸发结晶.| 温度/℃ | 0 | 10 | 20 | 40 | 60 | 80 |
| KIO3 g/100g水 | 4.60 | 6.27 | 8.08 | 12.6 | 18.3 | 24.8 |

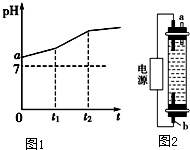 用惰性电极电解物质的量比为2:1的NaCl与NaHCO3混合溶液,溶液pH变化如图1所示.
用惰性电极电解物质的量比为2:1的NaCl与NaHCO3混合溶液,溶液pH变化如图1所示.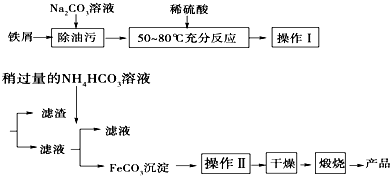



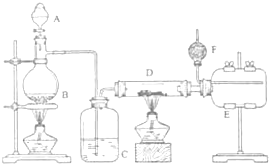 无水氯化铝是有机化工常用催化剂,其外观为白色固体,1780C时升华,极易潮解,遇 水后会发热并产生白雾.实验室用如图装置制备少量无水氯化铝,其反应原理为:2Al+6HCl(g)→2A1Cl3+3H2.完成下列填空:
无水氯化铝是有机化工常用催化剂,其外观为白色固体,1780C时升华,极易潮解,遇 水后会发热并产生白雾.实验室用如图装置制备少量无水氯化铝,其反应原理为:2Al+6HCl(g)→2A1Cl3+3H2.完成下列填空: