13.阿魏酸在食品、医药等方面有着广泛用途.一种合成阿魏酸的反应可表示为
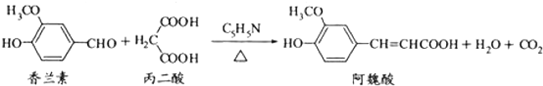
下列说法正确的是( )

下列说法正确的是( )
| A. | 可用酸性KmMO4溶液检测上述反应是否有阿魏酸生成 | |
| B. | 香兰素、阿魏酸均可与Na2CO3、NaOH溶液反应 | |
| C. | 通常条件下,香兰素、阿魏酸都能发生取代、加成、消去反应 | |
| D. | 1mol香兰素最多可以与4molH2发生加成反应 |
12.设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 0.1 mol组成为C2H6O的有机物,所含C-H键数目可能为0.5NA | |
| B. | 8.7 g MnO2与40 mL 10 mol/L的浓盐酸充分反应,生成的氯气分子数为0.1NA | |
| C. | 0.1 mol N2与0.3 mol H2在密闭容器中,在催化剂作用下充分反应,生成氨分子数为0.2NA | |
| D. | 标准状况下,22.4 L HF所含的分子数目为NA |
11.关于反应CaO+3C→CaC2+CO,下面哪种表述能最好地说明该反应是一个氧化还原反应( )
| A. | CaO失氧变为CaC2 | B. | C的状态发生了变化 | ||
| C. | Ca的化合价在反应前后发生了改变 | D. | C失去了电子,同时也得到了电子 |
10.下列说法错误的是( )
| A. | 已知反应2A(g)+B(g)?3C(g)△H>0,若温度降低,逆反应速率减小 | |
| B. | 在恒容容器中发生反应N2(g)+3H2(g)?2NH3(g),若往容器中充入He,正逆反应的速率均不变 | |
| C. | 当一定量的锌粉和4 mol•L-1的过量盐酸反应时,为了减慢反应速率,又不影响产生H2的总量,可向容器中加入一些水或硝酸钠溶液 | |
| D. | 对任何一个化学反应,温度发生变化,化学反应速率一定发生变化 |
5.下列关于元素周期表的说法正确的是( )
| A. | 第2周期与第3周期元素从左到右,最高正化合价均从+1逐渐增大至+7,0族元素一般是0价 | |
| B. | 3个长周期所含元素种数相同 | |
| C. | 不同主族的3、4周期元素原子序数的差可能不同 | |
| D. | 同周期从左到右,非金属元素含氧酸的酸性逐渐增强 |
4.钴的氧化物广泛应用于磁性材料及超导材料等领域.取一定量的钴的氧化物(其中钴的化合价为+2、+3价),用480mL 5mol•L-1盐酸恰好完全溶解固体,得到CoCl2溶液和4.48L(标准状况)黄绿色气体.通过计算可以确定该氧化物中Co、0的物质的量之比为( )
0 171783 171791 171797 171801 171807 171809 171813 171819 171821 171827 171833 171837 171839 171843 171849 171851 171857 171861 171863 171867 171869 171873 171875 171877 171878 171879 171881 171882 171883 171885 171887 171891 171893 171897 171899 171903 171909 171911 171917 171921 171923 171927 171933 171939 171941 171947 171951 171953 171959 171963 171969 171977 203614
| A. | 1:1 | B. | 2:3 | C. | 3:4 | D. | 5:6 |
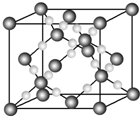 A、B、C、D、E、F为原子序数依次增大的短周期主族元素.A、C、D可形成常见的气态单质,A、E最外层电子数与其电子层数相等.B、F同主族,B元素基态原子核外电子平均分布在3个不同的能级上.C元素原子的最高能级上有3个未成对电子.F的一种单质与FD2晶体类型相同.
A、B、C、D、E、F为原子序数依次增大的短周期主族元素.A、C、D可形成常见的气态单质,A、E最外层电子数与其电子层数相等.B、F同主族,B元素基态原子核外电子平均分布在3个不同的能级上.C元素原子的最高能级上有3个未成对电子.F的一种单质与FD2晶体类型相同.