19.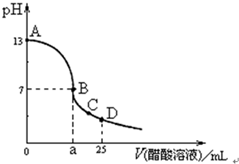 在25mL 0.1mol?L-1 NaOH溶液中逐滴加入0.2mol?L-1 CH3COOH溶液,曲线如图所示,下列判断正确的是( )
在25mL 0.1mol?L-1 NaOH溶液中逐滴加入0.2mol?L-1 CH3COOH溶液,曲线如图所示,下列判断正确的是( )
 在25mL 0.1mol?L-1 NaOH溶液中逐滴加入0.2mol?L-1 CH3COOH溶液,曲线如图所示,下列判断正确的是( )
在25mL 0.1mol?L-1 NaOH溶液中逐滴加入0.2mol?L-1 CH3COOH溶液,曲线如图所示,下列判断正确的是( )| A. | B点,a=12.5 | |
| B. | D点,c(Na+)=c(CH3COO-)+c(CH3COOH) | |
| C. | 在A、B间存在一点,此点水的电离程度最大 | |
| D. | 在C点升温,CH3COOH电离程度增大,CH3COO-的水解程度减小 |
18.H、D、T、H+可以用来表示( )
| A. | 化学性质不同的氢原子 | B. | 四种不同的元素 | ||
| C. | 氢元素的四种不同粒子 | D. | 四种不同的氢元素 |
16. 在密闭容器中发生可逆反应:3HCHO?(HCHO)3.在不同温度下,混合气体平均相对分子质量($\overline{{M}_{r}}$)与压强(p)的关系如图所示.下列有关推断正确的是( )
在密闭容器中发生可逆反应:3HCHO?(HCHO)3.在不同温度下,混合气体平均相对分子质量($\overline{{M}_{r}}$)与压强(p)的关系如图所示.下列有关推断正确的是( )
 在密闭容器中发生可逆反应:3HCHO?(HCHO)3.在不同温度下,混合气体平均相对分子质量($\overline{{M}_{r}}$)与压强(p)的关系如图所示.下列有关推断正确的是( )
在密闭容器中发生可逆反应:3HCHO?(HCHO)3.在不同温度下,混合气体平均相对分子质量($\overline{{M}_{r}}$)与压强(p)的关系如图所示.下列有关推断正确的是( )| A. | 若T2<T1,则△H<0 | B. | 平衡转化率:c<b=a | ||
| C. | 平衡常数:K(a)<K(c) | D. | $\overline{{M}_{r}}$=50时,HCHO的体积分数为$\frac{1}{3}$ |
15.下列说法正确的是( )
| A. | 在25℃、1.01×105Pa的条件下,22.4L H2中含有的分子数为0.1NA | |
| B. | 1L 1mol•L-1的CaCl2溶液中含Cl-的数目为2NA | |
| C. | 40g NaOH溶解在1L水中,所制得的100mL溶液中含Na+数为0.1NA | |
| D. | 22g CO2与标准状况下11.2L H2O含有相同分子数 |
12.将4.6gN2O4晶体放入容积为2L的容器中,升温到25℃,N2O4完全汽化并发生反应:N2O4?2NO2,反应达到平衡后,同温下测得压强为N2O4,完全汽化而未发生反应时压强的1.2倍,则下列不正确的是( )
| A. | 若升高温度,气体颜色将变深 | |
| B. | 平衡时NO2和N2O4的物质的量之比为1:2 | |
| C. | 平衡时混合气体的平均相对分子质量约为76.7 | |
| D. | 若相同温度下的另一容器中N2O4浓度为0.03mol/L,NO2浓度为0.01mol/L时,反应速率的关系为v正<v逆 |
11.下列有关实验的描述正确的是( )
| A. | 氢氧化钠固体保存在配有玻璃塞的细口瓶中 | |
| B. | 将SO2通入品红溶液或KMnO4酸性溶液均能使它们褪色,均可证明SO2有漂白性 | |
| C. | 不能在石英坩埚中熔化氢氧化钠 | |
| D. | 将金属钠在研钵中研成粉末,使钠与水反应的实验更安全 |
10.设NA代表阿伏加德罗常数(NA)的数值,下列说法正确的是( )
0 171661 171669 171675 171679 171685 171687 171691 171697 171699 171705 171711 171715 171717 171721 171727 171729 171735 171739 171741 171745 171747 171751 171753 171755 171756 171757 171759 171760 171761 171763 171765 171769 171771 171775 171777 171781 171787 171789 171795 171799 171801 171805 171811 171817 171819 171825 171829 171831 171837 171841 171847 171855 203614
| A. | 10 mL质量分数为98%的H2SO4,用水稀释至100 mL,H2SO4的质量分数为9.8% | |
| B. | 乙烯和环丙烷 (C3H6)组成的28 g混合气体中含有3NA个氢原子 | |
| C. | 标准状况下,22.4 L氯气与足量氢氧化钠溶液反应转移的电子数为NA | |
| D. | 将0.1 mol氯化铁溶于1 L水中,所得溶液含有0.1NA个Fe3+ |
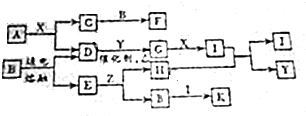
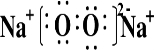 ;
; 一定量的NaOH和Na2CO3的混合物,溶于水配成100mL溶液,然后用2mol•L-1的盐酸滴定(指示剂先为酚酞试剂,后用甲基橙试液),得到如图所示图象,回答下列问题:
一定量的NaOH和Na2CO3的混合物,溶于水配成100mL溶液,然后用2mol•L-1的盐酸滴定(指示剂先为酚酞试剂,后用甲基橙试液),得到如图所示图象,回答下列问题: