19.(1)CO与H2在一定条件下可反应生成甲醇:CO(g)+2H2(g)═CH3OH(g).甲醇是一种燃料,可利用甲醇设计一个燃料电池,用稀硫酸作电解质溶液,多孔石墨作电极,该电池负极反应式为CH3OH(g)+H2O-6e-=CO2+6H+.
(2)高铁酸钾(K2FeO4)易溶于水,具有强氧化性,是一种新型水处理剂,高铁酸钾溶液长时间放置不稳定,会产生红褐色絮状物质及一种助燃性的气体,则该过程的离子方程式为4FeO42-+10H2O=4Fe(OH)3+8OH-+3O2↑.
(3)已知:
工业制镁时,电解MgCl2而不电解MgO的原因是MgO的熔点比MgCl2的熔点高,MgO熔融时耗费更多能源,增加成本;制铝时,电解Al2O3而不电解AlCl3的原因是AlCl3是共价化合物,熔融态时不电离,难导电.
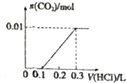
(4)为测定三草酸合铁酸钾晶体中草酸根的含量,通常将其配成溶液再用H2SO4酸化,滴加KMnO4溶液将草酸根恰好全部氧化成CO2,MnO4-同时被还原为Mn2+此反应不要(要/不要)外加指示剂,达到滴定终点的现象为当待测液中出现紫红色,且振荡后半分钟内不再褪色,就表明到了终点.
(2)高铁酸钾(K2FeO4)易溶于水,具有强氧化性,是一种新型水处理剂,高铁酸钾溶液长时间放置不稳定,会产生红褐色絮状物质及一种助燃性的气体,则该过程的离子方程式为4FeO42-+10H2O=4Fe(OH)3+8OH-+3O2↑.
(3)已知:
| 化合物 | MgO | Al2O3 | MgCl2 | AlCl3 |
| 类型 | 离子化合物 | 离子化合物 | 离子化合物 | 共价化合物 |
| 熔点/℃ | 2800 | 2050 | 714 | 191 |
(4)为测定三草酸合铁酸钾晶体中草酸根的含量,通常将其配成溶液再用H2SO4酸化,滴加KMnO4溶液将草酸根恰好全部氧化成CO2,MnO4-同时被还原为Mn2+此反应不要(要/不要)外加指示剂,达到滴定终点的现象为当待测液中出现紫红色,且振荡后半分钟内不再褪色,就表明到了终点.
18.X、Y、Z都是气体,在减压或升温后,Z的物质的量都会增大的反应是( )
| A. | X+Y?3Z(正反应吸热) | B. | 2X+Y?2Z(正反应吸热) | ||
| C. | X+Y?2Z(正反应吸热) | D. | X+2Y?4Z(正反应放热) |
11.下列各组离子能在指定溶液中,大量共存的是( )
| A. | 能使pH试纸呈红色的溶液中:NH4+,Al3+,I-,NO3- | |
| B. | 加入Al能放出H2的溶液中:Cl-,HCO3-,NO3-,NH4+ | |
| C. | pH=1的澄清透明溶液中:Cu2+,NH4+,K+,SO42- | |
| D. | FeCl3溶液中:SCN-,Na+,AlO2-,K+ |
10.下列有关物质的性质或应用的说法正确的是( )
0 171653 171661 171667 171671 171677 171679 171683 171689 171691 171697 171703 171707 171709 171713 171719 171721 171727 171731 171733 171737 171739 171743 171745 171747 171748 171749 171751 171752 171753 171755 171757 171761 171763 171767 171769 171773 171779 171781 171787 171791 171793 171797 171803 171809 171811 171817 171821 171823 171829 171833 171839 171847 203614
| A. | 晶体硅具有半导体性质,可用于生成光导纤维 | |
| B. | 用Na2O2漂白过的织物,麦秆日久又渐渐变成黄色 | |
| C. | K2FeO4具有氧化性,可用于自来水的杀菌消毒 | |
| D. | 浓硫酸具有较强酸性,常用作淀粉水解的催化剂 |
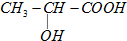 )及其盐广泛应用于食品、医药、化工等领域.有一种制备乳酸方法如下:
)及其盐广泛应用于食品、医药、化工等领域.有一种制备乳酸方法如下: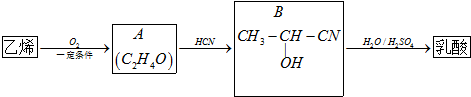
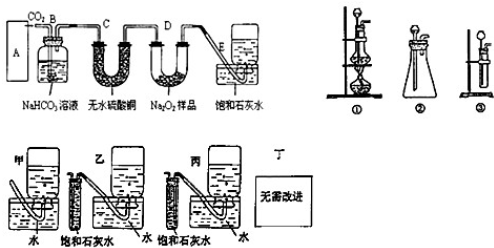
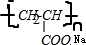 .
.

 短周期主族元素A、B、C、D、E、F的原子序数依次增大,已知A的原子半径比B的小,B在反应中既不容易得到电子也不容易失去电子,C元素的气态氢化物和其最高价氧化物对应水化物能化合生成盐,元素D的原子最外层电子数是其电子层数的3倍,E与A同一主族,F常用于制半导体.
短周期主族元素A、B、C、D、E、F的原子序数依次增大,已知A的原子半径比B的小,B在反应中既不容易得到电子也不容易失去电子,C元素的气态氢化物和其最高价氧化物对应水化物能化合生成盐,元素D的原子最外层电子数是其电子层数的3倍,E与A同一主族,F常用于制半导体.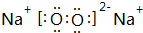
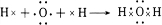 ,写出A2D与X反应的化学方程式,并用单线桥标出电子转移
,写出A2D与X反应的化学方程式,并用单线桥标出电子转移