题目内容
15.过氧化钠是一种淡黄色固体,它能与二氧化碳反应生成氧气,它与二氧化碳反应的化学方程式为:2Na2O2+2CO2═2Na2CO3+O2.某学生为了验证这一实验,以足量的大理石、足量的盐酸和1.95克过氧化钠样品为原料,制取O2,设计出如下实验装置: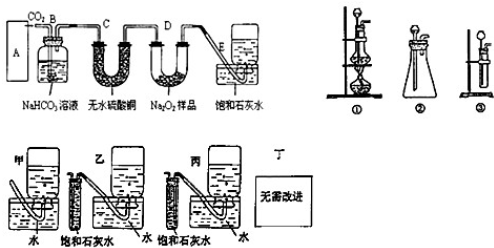
(1)A中制取CO2的装置,应从下列图①、②、③中选哪个图:②③
(2)B装置的作用是除去CO2中的HCl,C装置内可能出现的现象是无水硫酸铜变蓝.为了检验E中收集到的气体,在取出集气瓶后,用带火星的木条伸入集气瓶内,木条会出现复燃.
(3)若E中的石灰水出现出现轻微白色浑浊,请说明原因:还有未反应的CO2
(4)反应完毕时,若测得E中的集气瓶收集到的气体为250mL(标准状况下),当装置的气密性良好的情况下,实际收集到的氧气体积比理论计算值小(答大或小),相差约30mL(取整数值,所用数据均在标准状况下测定).
分析 (1)依据反应物状态和反应条件选择发生装置;
(2)浓盐酸的易挥发制取的二氧化碳中含有氯化氢杂质,结合氯化氢、二氧化碳性质除杂;无水硫酸铜容易结合水生成蓝矾;过氧化钠与二氧化碳反应生成碳酸钠和氧气,依据氧气能够支持燃烧的性质选择检验方法;
(3)能该题中够使石灰水变浑浊的只有二氧化碳;
(4)根据过氧化钠的质量可以生成氧气的体积,理论生成气体的体积-实际氧气的体积=差值.
解答 解:(1)实验室制备二氧化碳用的原料为碳酸钙固体与盐酸液体,反应条件不需要加热,所以可以选择装置
②③;
故答案为:②③;
(2)浓盐酸的易挥发制取的二氧化碳中含有氯化氢杂质,二氧化碳在饱和碳酸氢钠溶液中溶解度,不大,氯化氢与饱和碳酸氢钠反应生成二氧化碳,所以可以选择饱和碳酸氢钠溶液除去杂质氯化氢;
无水硫酸铜容易结合水生成蓝矾,从装置B中出来的气体含有水蒸气,所以看到现象为:无水硫酸铜变蓝;
过氧化钠与二氧化碳反应生成碳酸钠和氧气,氧气能够支持燃烧,所以检验氧气的方法为:用带火星的木条伸入集气瓶内,木条会出现复燃;
故答案为:除去CO2中的HCl 无水硫酸铜变蓝 带火星 复燃;
(3)若E中的石灰水出现出现轻微白色浑浊,说明:还有未反应的CO2;
故答案为:还有未反应的CO2;
(4)1.95g过氧化钠的物质的量为$\frac{1.95g}{78g/mol}$=0.025mol,设过氧化钠完全反应生成氧气的体积为v,依据反应方程式得:
2Na2O2----O2;
2mol 22.4L
0.025mol v
v=0.28L=280mL>250mL,所以实际收集到的氧气体积比理论计算值小;
280mL-250mL=30mL;
故答案为:小;30.
点评 本题考查了二氧化碳制备、净化及性质检验,明确实验原理及过氧化钠性质是解题关键,题目难度中等.

 阅读快车系列答案
阅读快车系列答案| A. | 都能通过化合反应实现 | B. | 都能通过置换反应实现 | ||
| C. | 都能通过与单质反应实现 | D. | 变化前后元素化合价都发生了改变 |
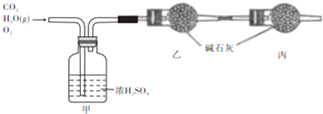
| 质量 物质 | 实验前 | 实验后 |
| 甲的质量/g | 101.1 | l03.0 |
| 乙的质量/g | 82.0 | 86.4 |
(1)该燃料分了中碳、氢原了的数目比为1:3.
(2)已知该燃料只含一种分了且分子的相对分子质量不超过50,则其分子式为C2H6O.
(3)符合(2)中所得分子式的有两种有机物,其鉴別可采用化学方法及物理方法.下列鉴別方法中不能对二者进行鉴別的是BC(填选项序号).
A.利用金属钠或金属钾
B.利用燃烧法
C.利用红外光谱
D.利用核磁共振氢谱
(4)聚酯树脂(聚对苯二甲酸乙二酯树脂.简号为PFT)可制造聚酯纤维,聚酯薄膜及多种塑料制品等,其两种单体的生产流程为:
I.利用常见生物质生产F:
天然高分子化合物B→C(分子式C6H12O6)→A→D(C2H4)→E→F
Ⅱ.用甲笨歧化法生产对二甲苯:
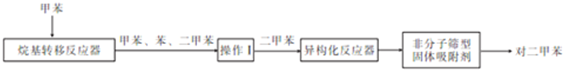
以醋酸钴和醋酸锰为催化剂将对二甲苯分步氧化产生M:

已知:
苯,密度0.877g.mL-1,熔点5.5℃,沸点80.1℃.
甲笨,密度0.866 k•mL-1,熔点一95℃,沸点110.6℃
二甲笨,为无色透明液体.沸点为137〜140℃
①C中含有的官能团的名称是羟基和醛基.
A→D→E→F的反应类型分別为消去反应、加成反应、取代反应.
②操作Ⅰ的名称是蒸馏:
对二甲笨分步氧化阶段.由于第二个甲基不易氧化,反应过程易停止在对甲基笨甲酸阶段.写出符合下列全部条件的对甲基笨甲酸的所有同分异构体的结构简式:
 、
、 .
.a.能与NaOH溶液反应
b.不与NaHCO3溶液反应放出气体
c.为芳香族化合物
d.不与银氨银溶液作用生成Ag
c.不与FeCl3溶液发生显色反应
③F、M生成PET的化学反应方程式为:
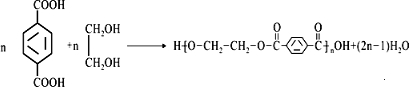 .
. | A. | 晶体硅具有半导体性质,可用于生成光导纤维 | |
| B. | 用Na2O2漂白过的织物,麦秆日久又渐渐变成黄色 | |
| C. | K2FeO4具有氧化性,可用于自来水的杀菌消毒 | |
| D. | 浓硫酸具有较强酸性,常用作淀粉水解的催化剂 |
| 步骤 | 操作 | 现象 |
| I | 向2mL 1mol•L-1FeCl3溶液中加入一定量的Na2SO3溶液 | 溶液由棕黄色变为红褐色, 并有少量刺激性气味的气体逸出 |
(2)分析红褐色产生的原因.
①甲同学认为步骤I中溶液呈红褐色是因为生成了Fe(OH)3,用化学平衡移动原理解释溶液呈红褐色的原因:Fe3++3H2O═Fe(OH)3+3H+,加入Na2SO3后,c(H+)下降,平衡正向移动,生成Fe(OH)3.
②乙同学认为可能是发生了氧化还原反应,完成并配平其反应的离子方程式:
□Fe3++□SO32-+□H2O═□F e2++□SO42-+□2H+
乙同学查阅资料得知:
| 1Fe2+与SO32-反应生成墨绿色的絮状沉淀FeSO3; 2墨绿色的FeSO3与黄色的FeCl3溶液混合后,溶液呈红褐色. |
| 步骤 | 操作 | 现象 |
| II | 用激光笔照射步骤I中的红褐色溶液 | 出现“丁达尔效应” |
(4)为进一步确认Na2SO3溶液与FeCl3溶液反应的情况,乙同学设计并完成了如下实验:
| 步骤 | 操作 | 现象 |
| III | 向1mol•L-1的FeCl3溶液中通入一定量的SO2 | 溶液由黄色变为红褐色 |
| IV | 用激光笔照射步骤III中的红褐色溶液 | 没有出现“丁达尔效应” |
a.K3[Fe(CN)6]溶液 b.KSCN溶液 c.KMnO4溶液
②已知H2SO3是弱酸,请结合电离方程式说明步骤III中出现红褐色的原因:H2SO3?H++HSO3-、HSO3-?H++SO32-,SO32-与被还原生成的Fe2+结合为FeSO3,与剩余的FeCl3溶液混合而呈现红褐色.
(5)结论:由上述实验得知,甲、乙两同学所持观点均正确.
| A. | N2O4的体积分数减小 | B. | NO2的转化率提高 | ||
| C. | 平均相对分子质量增大 | D. | 颜色变深 |
| A. | 在海轮外壳连接锌块保护外壳不受腐蚀是采用了牺牲阴极的阳极保护法 | |
| B. | 石油的分馏、煤的液化、汽化都是物理变化 | |
| C. | 干馏煤可以得到甲烷、苯和氨等重要化工原料 | |
| D. | 纤维素、蔗糖、葡萄糖和脂肪在一定条件下都可以发生水解反应 |
| A. | F2、Cl2、Br2、I2的氧化性逐渐减弱,密度逐渐增大,熔沸点逐渐升高 | |
| B. | HF、HCl、HBr、HI的热稳定性逐渐减弱 | |
| C. | F-、Cl-、Br-、I-的还原性逐渐增强,颜色逐渐变深 | |
| D. | 与水反应由难到易:F2>Cl2>Br2>I2 |
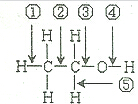 乙醇的分子结构为(如图):乙醇与钠反应时,断开的键是④;与HX反应时,断开的键是③;分子内脱水生成乙烯时,断开的键是①③;在铜催化作用下发生催化氧化反应时,断开的键是④⑤;酯化反应时,断开的键是④.
乙醇的分子结构为(如图):乙醇与钠反应时,断开的键是④;与HX反应时,断开的键是③;分子内脱水生成乙烯时,断开的键是①③;在铜催化作用下发生催化氧化反应时,断开的键是④⑤;酯化反应时,断开的键是④.