题目内容
18.X、Y、Z都是气体,在减压或升温后,Z的物质的量都会增大的反应是( )| A. | X+Y?3Z(正反应吸热) | B. | 2X+Y?2Z(正反应吸热) | ||
| C. | X+Y?2Z(正反应吸热) | D. | X+2Y?4Z(正反应放热) |
分析 减压平衡向气体体积增大的方向移动,升温平衡向吸热反应方向移动,Z的物质的量都会增大,说明该反应为气体体积增大的吸热反应,据此分析.
解答 解;因为减压平衡向气体体积增大的方向移动,升温平衡向吸热反应方向移动,Z的物质的量都会增大,说明该反应为气体体积增大的吸热反应,所以A正确;
故选:A.
点评 本题主要考查了平衡的移动原理,注意减压平衡向气体体积增大的方向移动,升温平衡向吸热反应方向移动,比较简单.

练习册系列答案
相关题目
19.有一在空气中暴露过久的NaOH固体,经分析得知其含水,Na2CO3•10H2O,Na2CO3,其余为NaOH,取此样品10.8g溶于100mL 1mol•L-1的硫酸里,剩余酸需加入0.4g NaOH刚好中和完全,由此可知蒸发中和后的溶液可得固体质量( )
| A. | 14.2g | B. | 19.8g | C. | 21.3g | D. | 无法计算 |
9.下列一些生活中常见物质的相关说法正确的是( )
| A. | 明矾和纯碱可分別用于水的消毒,洗涤油污 | |
| B. | 鸡蛋清溶液中加人饱和硫酸钠溶液•生成的沉淀物不能再溶解 | |
| C. | 紫色酸性离高锰酸钾溶液中加人植物油充分振荡后,溶液液分层且上层为紫色 | |
| D. | “84”消毒液溶液中滴加醋酸.KI淀粉溶液振荡后溶液变蓝色 |
3.如图所示,试管中的物质M可能是( )
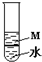

| A. | 四氯化碳 | B. | 乙醇 | C. | 已烷 | D. | 溴苯 |
10.下列说法正确的是( )
| A. | 将AlCl3溶液、Na2SO3溶液蒸干并灼烧可分期得到A12O3、Na2SO3 | |
| B. | 在溶液的稀释过程中,离子浓度有的可能增大,有的可能减小,有的可能不变 | |
| C. | Ksp(BaSO4)=1.08×10-10,Ksp(BaCO3)=8.1×10-9,则沉淀BaSO4不可能转化为BaCO3 | |
| D. | 0.1mo1•L-1CH3COOH溶液在稀释过程中$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$将变小 |
7. 如图是某学校实验室买回的硫酸试剂标签上的部分内容,据此判断下列说法正确的是( )
如图是某学校实验室买回的硫酸试剂标签上的部分内容,据此判断下列说法正确的是( )
 如图是某学校实验室买回的硫酸试剂标签上的部分内容,据此判断下列说法正确的是( )
如图是某学校实验室买回的硫酸试剂标签上的部分内容,据此判断下列说法正确的是( )| A. | 该硫酸的浓度为18.4mol•L-1 | |
| B. | 配制200mL 4.6mol•L-1的稀硫酸需该硫酸50mL | |
| C. | 配制100g10%的硫酸需要用到的仪器有胶头滴管、烧杯、玻璃棒、100mL量筒、天平 | |
| D. | 稀释该浓硫酸时可直接把水加入浓硫酸中 |