18.将一定量的锌与100mL 18.5mol•L-1浓硫酸充分反应后,锌完全溶解,同时生成气体A 22.4L(标准状况).将反应后的溶液稀释至1L,测得溶液的pH=1,则下列叙述中正确的是( )
| A. | 气体A为SO2 | B. | 反应中共消耗Zn 97.5 g | ||
| C. | 气体A中SO2和H2的体积比为4:1 | D. | 反应中共转移3 mol电子 |
15.下列离子方程式中正确的是( )
| A. | 氢氧化钡溶液与稀硫酸混合:Ba2++OH-+H++SO42-═BaSO4↓+H2O | |
| B. | 少量SO2通入到漂白粉溶液中:Ca2++2ClO-+SO2+H2O=CaSO3↓+2HClO | |
| C. | 氯化铝溶液与过量的氨水反应:Al3++4NH3•H2O=AlO2-+4NH4++2H2O | |
| D. | 往明矾溶液中加入氢氧化钡溶液至SO42-完全沉淀:Al3++2SO42-+2 Ba2++4OH-═AlO2-+2BaSO4↓+2H2O |
14.钢铁“发蓝”是将钢铁制品浸到某些氧化性的溶液中,在钢铁的表面形成一层四氧化三铁的技术过程.其中一种办法是将钢铁制品浸到亚硝酸钠和浓氢氧化钠的混合溶液中加热到130℃反应.其过程可以用如下化学方程式表示:
①3Fe+NaNO2+5NaOH=3Na2FeO2+H2O+NH3↑;
②Na2FeO2+NaNO2+H2O═Na2Fe2O4+NH3↑+NaOH (未配平);
③Na2FeO2+Na2Fe2O4+2H2O=Fe3O4+4NaOH;
下列说法不正确的是( )
①3Fe+NaNO2+5NaOH=3Na2FeO2+H2O+NH3↑;
②Na2FeO2+NaNO2+H2O═Na2Fe2O4+NH3↑+NaOH (未配平);
③Na2FeO2+Na2Fe2O4+2H2O=Fe3O4+4NaOH;
下列说法不正确的是( )
| A. | 碱性条件下,NaNO2的氧化性比Na2FeO2、Na2Fe2O4都强 | |
| B. | 反应 ①、②、③均是氧化还原反应 | |
| C. | 反应 ②配平后,H2O的化学计量数是5 | |
| D. | 整个反应过程中每有16.8g Fe参加反应转移0.8mol电子 |
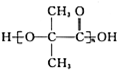
12.X、Y都是芳香族化合物,1molX水解得到1molY和2mol醋酸.Y相对分子质量介于100~150之间,且碳和氢两种元素总质量分数为65.2%.X溶液能发生银镜反应,向Y水溶液中滴加NaHCO3无气泡,滴加FeCl3溶液显紫色.下列说法正确的是( )
0 171505 171513 171519 171523 171529 171531 171535 171541 171543 171549 171555 171559 171561 171565 171571 171573 171579 171583 171585 171589 171591 171595 171597 171599 171600 171601 171603 171604 171605 171607 171609 171613 171615 171619 171621 171625 171631 171633 171639 171643 171645 171649 171655 171661 171663 171669 171673 171675 171681 171685 171691 171699 203614
| A. | X、Y相对分子质量之差为84 | |
| B. | X中含有HCOO-,Y中含有-OH | |
| C. | Y的分子式为:C7H8O3 | |
| D. | 若X中有四种氢,则满足条件的X可能有两种 |

 ,G是一种高分子,可用于制造隐形眼镜的材料.H为六元环酯.
,G是一种高分子,可用于制造隐形眼镜的材料.H为六元环酯.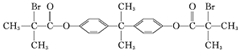 .
. .
. .
.
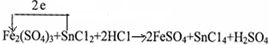 .
.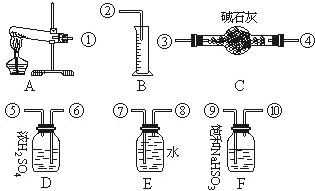 CuSO4在一定条件下发生如下分解:CuSO4═CuO+SO2+SO3+O2,有人设计通过实验测定反应产生的SO2,SO3,O2的物质的量的方法,并经计算确定该条件下分解反应式各物质的系数.实验可能需要的仪器如图所示:
CuSO4在一定条件下发生如下分解:CuSO4═CuO+SO2+SO3+O2,有人设计通过实验测定反应产生的SO2,SO3,O2的物质的量的方法,并经计算确定该条件下分解反应式各物质的系数.实验可能需要的仪器如图所示: