15.下列反应的离子方程式书写正确的是( )
| A. | 胃舒平(主要含氢氧化铝)治疗胃酸过多:OH-+H+═H2O | |
| B. | 醋酸除水垢:2H++CaCO3═Ca2++H2O+CO2↑ | |
| C. | 敞口的澄清石灰水变质:Ca2++2OH-+2CO2═Ca(HCO3)2 | |
| D. | 稀盐酸除铁锈:6H++Fe2O3═2Fe3++3H2O |
14.不能用离子方程式Ba2++SO42-═BaSO4↓表示的化学反应有( )
| A. | BaCl2溶液与稀硫酸反应 | B. | Ba(OH)2溶液与Na2SO4溶液反应 | ||
| C. | Ba(OH)2溶液与NaHSO4溶液反应 | D. | Ba(NO3)2溶液与MgSO4溶液反应 |
13.下列叙述中,正确的是( )
| A. | 标准状况下,Cl2的摩尔质量为71g | |
| B. | 氧化还原反应一定有氧元素参加 | |
| C. | 国际上规定,0.012kg 12C所含有的碳原子数约为1mol | |
| D. | Na2CO3属于钠盐,又属于碳酸盐是用交叉分类法分类的 |
12.下列实验操作中不正确的是( )
| A. | 蒸馏时,应将温度计水银球置于蒸馏烧瓶支管口处 | |
| B. | 定容时,如果加水超过了刻度线,则可用胶头滴管吸出多余部分 | |
| C. | 配制稀硫酸时,先在烧杯中加入一定量水,再沿玻璃棒慢慢加入浓硫酸 | |
| D. | 称量NaOH时,NaOH置于小烧杯中放在托盘天平左盘,砝码放在右盘 |
11.装运浓硫酸的储运罐应贴的标志是( )
| A. |  | B. |  | C. |  | D. |  |
9.原子序数逐渐增大的元素A、B、C、D、E、F的有关信息如下:
根据以上表格信息回答:
(1)元素F在周期表中的位置是第四周期IB族,E形成的低价离子的电子排布式为1s22s22p63s23p63d10.
(2)A、C的氢化物沸点较高的是(用所形成的氢化物表示)H2O,A、B、C的第一电离能大小顺序是(用元素符号表示)N>O>C.
(3)A与氢元素形成的A2H2含有的σ键、π键数目之比为3:2.
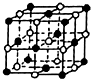
(4)KCl的晶胞如图:“●K,○Cl”,则该晶胞中含K+为4个,已知晶胞参数为:629.8pm(1pm=10-12m),求KCl晶体的密度为$\frac{4×(39+35.5)}{6.02×1{0}^{23}×(629.8×1{0}^{-10})^{3}}$g/cm3(只写出表达式,不要求计算结果).
(5)用惰性电极电解FCl2溶液时,在阴极除了析出红色固体外,还析出白色固体,经检验白色固体为FCl,请写出析出白色固体的阴极反应式Cu2++Cl-+e-=CuCl.
0 171457 171465 171471 171475 171481 171483 171487 171493 171495 171501 171507 171511 171513 171517 171523 171525 171531 171535 171537 171541 171543 171547 171549 171551 171552 171553 171555 171556 171557 171559 171561 171565 171567 171571 171573 171577 171583 171585 171591 171595 171597 171601 171607 171613 171615 171621 171625 171627 171633 171637 171643 171651 203614
| 代号 | 信息 |
| A | 原子最外层电子数为内层电子数的2倍 |
| C | 形成的一种单质可抵御紫外线对地球生物的伤害 |
| D | 是一种非金属元素,属于卤族之一,形成的气体常温常压下为黄绿色 |
| E | 单质是生活中使用最广泛的金属 |
| F | 形成的一种化合物可用于醛基的检验 |
(1)元素F在周期表中的位置是第四周期IB族,E形成的低价离子的电子排布式为1s22s22p63s23p63d10.
(2)A、C的氢化物沸点较高的是(用所形成的氢化物表示)H2O,A、B、C的第一电离能大小顺序是(用元素符号表示)N>O>C.
(3)A与氢元素形成的A2H2含有的σ键、π键数目之比为3:2.
(4)KCl的晶胞如图:“●K,○Cl”,则该晶胞中含K+为4个,已知晶胞参数为:629.8pm(1pm=10-12m),求KCl晶体的密度为$\frac{4×(39+35.5)}{6.02×1{0}^{23}×(629.8×1{0}^{-10})^{3}}$g/cm3(只写出表达式,不要求计算结果).

(5)用惰性电极电解FCl2溶液时,在阴极除了析出红色固体外,还析出白色固体,经检验白色固体为FCl,请写出析出白色固体的阴极反应式Cu2++Cl-+e-=CuCl.
