5.氨基酸是组成蛋白质的基本结构单位,下列说法正确的是( )
| A. | 组成蛋白质的氨基酸一定是α-氨基酸 | |
| B. | 氨基酸都含有手性碳原子 | |
| C. | 氨基酸具有两性,蛋白质不具有两性 | |
| D. | 天然氨基酸大部分能溶于水,难溶于乙醇、乙醚 |
2.下列有关元素的性质及递变规律中错误的是( )
| A. | IA族与VIIA族元素间可形成共价化合物或离子化合物 | |
| B. | 第三周期元素从左到右,最高正价从+1 递增到+7 | |
| C. | 同主族元素的简单阴离子还原性越强,其在水中越容易水解 | |
| D. | 同周期的主族金属元素的化合价越高,其原子失电子能力越弱 |
20.在某一化学反应中,反应物X的浓度在5s内从2.0mol/L变成0.5mol/L,在这5s内X的化学反应速率为( )
| A. | 0.3 | B. | 0.3 mol/(L•s) | C. | 0.4 mol(L•s)-1 | D. | 0.04 mol/L |
17.常温下,下列溶液的pH或微粒的物质的量浓度关系正确的是( )
0 171408 171416 171422 171426 171432 171434 171438 171444 171446 171452 171458 171462 171464 171468 171474 171476 171482 171486 171488 171492 171494 171498 171500 171502 171503 171504 171506 171507 171508 171510 171512 171516 171518 171522 171524 171528 171534 171536 171542 171546 171548 171552 171558 171564 171566 171572 171576 171578 171584 171588 171594 171602 203614
| A. | 某物质的溶液中由水电离出的c(H+)=1×10-amol/L,若a>7时,则该溶液的pH一定为14-a | |
| B. | 某溶液中存在的离子有S2-、HS-、OH-、Na+、H+,则离子浓度一定是c(Na+)>c(S2-)>c(OH-)>c(HS-)>c(H+) | |
| C. | 将0.2 mol/L的某一元酸HA溶液和0.1mol/L NaOH溶液等体积混合后溶液pH大于7,则反应后的混合液:2c(OH-)=2c(H+)+c(HA)-c(A-) | |
| D. | ①Na2CO3溶液②CH3COONa溶液③NaOH溶液,若3种溶液pH均为9,则它们物质的量浓度大小顺序是①>②>③ |
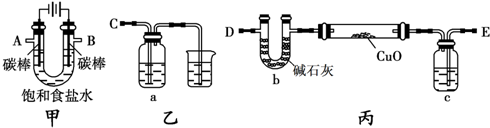

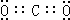 ;I中所含化学键类型离子键、共价键,气体D所含元素在周期表中的位置第三周期ⅤⅡA族
;I中所含化学键类型离子键、共价键,气体D所含元素在周期表中的位置第三周期ⅤⅡA族