��Ŀ����
3���������ʵ��Ʊ��빤ҵ����������ǣ���������SiO2$��_{����}^{��̿}$�ֹ�$��_{����}^{Cl_{2}}$SiCl4 $��_{����}^{H_{2}}$Si���ߴ��ȣ�
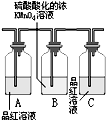
��Ũ����$��_{��}^{MnO_{2}}$Cl2$\stackrel{ʯ����}{��}$Ư��
��MgCl2$\stackrel{��������}{��}$��ˮ2$��_{����}^{���}$Mg
�ܱ���NaCl��Һ$\stackrel{NH_{3}��CO_{2}}{��}$NaHCO3����$\stackrel{����}{��}$Na2CO3��
| A�� | �٢� | B�� | �٢� | C�� | �ڢ� | D�� | �ڢ� |
���� �ٹ�ҵ�ö���������̼��Ӧ��ȡ�ֹ裬�ֹ���������Ӧ�������Ȼ��裬Ȼ����������ԭ���Ȼ������ᴿ�裻
�ڹ�ҵ�õ�ⱥ��ʳ��ˮ������ȡ������
�۹�ҵ����Mg�Ĺ��̣�MgC12��Һ����MgC12��Һ�������ᾧ�õ�MgC12•6H2O��Ȼ��MgC12•6H2O��һ�������¼��ȵõ���ˮMgC12��MgCl2•6H2O$\frac{\underline{\;����\;}}{\;}$MgCl2+6H2O����������ڵ��Ȼ�þ�ɵõ�Mg��MgCl2$\frac{\underline{\;���\;}}{\;}$Mg+Cl2����
�������Ƽ����ʹ����ͨ�뱥��ʳ��ˮ�ж��ɰ���ˮ����ͨ�������̼�����ܽ�Ƚ�С��̼�����Ƴ������Ȼ����Һ���仯ѧ��Ӧԭ���ǣ�NH3+CO2+H2O+NaCl�����ͣ�=NaHCO3��+NH4Cl���������ˡ�ϴ�ӵõ���NaHCO3С���壬�ټ��������Ƶô����Ʒ��2NaHCO3$\frac{\underline{\;\;��\;\;}}{\;}$Na2CO3+CO2��+H2O��
��� �⣺�ٹ�ҵ��ȡ�ֹ衢�ᴿ��Ĺ���Ϊ��SiO2$��_{����}^{��̿}$�ֹ�$��_{����}^{Cl_{2}}$SiCl4 $��_{����}^{H_{2}}$Si���ߴ��ȣ�������ȷ��
�ڹ�ҵ�õ�ⱥ��ʳ��ˮ������ȡ����������ͨ��ʯ������ȡƯ�ۣ��ʴ���
�۹�ҵ����Mg�Ĺ�ҵ���̣�MgC12��Һ��MgCl2��aq��$\stackrel{�����ᾧ}{��}$MgC12•6H2O$\stackrel{HCl}{��}$��ˮMgCl2$\stackrel{���}{��}$Mg���ʴ���
�������Ƽ�Ĺ�ҵ���̣�����NaCl��Һ$\stackrel{NH_{3}��CO_{2}}{��}$NaHCO3����$\stackrel{����}{��}$Na2CO3������ȷ��
��ѡ��B��
���� ���⿼�������ʵĹ�ҵ�Ʊ�����Ϥ���ʵ����ʣ������Ʊ�ԭ���ǽ���ؼ�����Ŀ�ѶȲ���

 Ӣ�ŵ��ϵ�д�
Ӣ�ŵ��ϵ�д� ������������Ծ�ϵ�д�
������������Ծ�ϵ�д���һ���Ʊ�����������
 +C2H5OH$\stackrel{H_{2}SO_{4}}{?}$
+C2H5OH$\stackrel{H_{2}SO_{4}}{?}$ +H2O
+H2O������ʵIJ����������������
| �е㣨�棩 | �ܶȣ�g•cm-3�� | |
| ������ | 249 | 1.2659 |
| ���������� | 212.6 | 1.05 |
| �Ҵ� | 78.5 | 0.7893 |
| ������ | 80.8 | 0.7785 |
| ���� | 34.51 | 0.7318 |
| �����顢�Ҵ���ˮ������ | 62.1 |
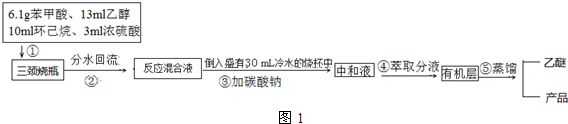
��1���Ʊ�������������ͼ2װ������ʵ���B����ӦҺ�еĻ������ڱ�ʵ���е����ã�ͨ���γ�ˮ-�Ҵ�-��������Ԫ������������ɵ�ˮ���ٽ�������Ӧ��������У�

��2������ڿ����¶���65��70�滺������Һ���������ˮ���������ϡ�������Һ�壬ֱ����Ӧ��ɣ�ֹͣ���ȣ��ų���ˮ���е��²�Һ��������ȣ�����������Ҵ��ͻ����飮
��Ӧ��ɵı�־�Ƿ�ˮ�����²㣨ˮ�㣩Һ�治�����ߣ�
��3�������̼���Ƶ��������кͱ���������ᣬ̼���ƹ���������·��������ԭ�������������ĭ�IJ�����ʹҺ�������
��4������ܽ��кͺ��Һ��ת���Һ©���ֳ��л��㣬ˮ����25mL������ȡ��Ȼ��ϲ����л��㣬����ˮMgSO4������ѵ�������ȡ��ˮ�����ܽ�ı�������������߲��ʣ�
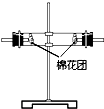
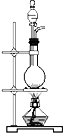
��5���������������У�ͼ3װ����õ���bd�����ţ�������ʱ�ȵ����������ѣ���������ʱ��ò���ˮԡ���ȣ�ˮԡ���ȡ�ֱ�Ӽ��ȡ���ԡ���ȣ���

�������Ʊ�������ͭ
����������뵽�Ҵ���ˮ�Ļ���ܼ��У�����ܽ����Cu��OH��2��δ��Ȼ��ˮԡ���ȣ���70��80���±���2��3Сʱ�����ȹ��ˣ���Һ������ȴ������������ͭ���壬���ˡ�ϴ�ӡ�����õ���Ʒ��
��6������ܼ����Ҵ�������������������ܽ�ȣ����ڳ�ַ�Ӧ�����ȹ��˵�ԭ����ͭ��ȴ���ᾧ�������粻���ȹ��˻���ʧ��Ʒ
��7����ʵ��������ҩƷ���ܴ���������ͭʹ�õ���D
A������ͭ����B������ͭ���� C����ʽ̼��ͭ����D������ͭ
��8��ϴ�ӱ�����ͭ����ʱ������ϴ�Ӽ�����ʵ���C
A����ˮ B����ˮ C���Ҵ� D���Ҵ�ˮ�����Һ��
| A�� | �����£�23g�Ҵ��ͼ���Ļ�����к���O-H������ĿΪ0.5NA | |
| B�� | 40g SiC�к���Si-C������ĿΪ2NA | |
| C�� | ��״���£�22.4L��ȩ���з��ӵ���ĿΪNA | |
| D�� | 2mol�����ᣨ9��12-ʮ��̼��ϩ�ᣬC17H31COOH���к���˫������Ŀ��4NA |



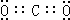 ��I��������ѧ���������Ӽ������ۼ�������D����Ԫ�������ڱ��е�λ�õ������ڢ���A��
��I��������ѧ���������Ӽ������ۼ�������D����Ԫ�������ڱ��е�λ�õ������ڢ���A��