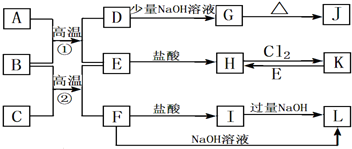
12. 向体积为0.5L的AlCl3溶液中逐渐加入某浓度的NaOH溶液,得到的沉淀随NaOH溶液体积的变化如图所示.下列结果不正确的是( )
向体积为0.5L的AlCl3溶液中逐渐加入某浓度的NaOH溶液,得到的沉淀随NaOH溶液体积的变化如图所示.下列结果不正确的是( )
 向体积为0.5L的AlCl3溶液中逐渐加入某浓度的NaOH溶液,得到的沉淀随NaOH溶液体积的变化如图所示.下列结果不正确的是( )
向体积为0.5L的AlCl3溶液中逐渐加入某浓度的NaOH溶液,得到的沉淀随NaOH溶液体积的变化如图所示.下列结果不正确的是( )| A. | 反应过程中,沉淀最多时的质量为78g | |
| B. | 反应过程中,Al3+离子有$\frac{1}{3}$转化为Al(OH)3沉淀,则加入的NaOH溶液的体积可能为3.5L | |
| C. | AlCl3溶液的浓度为2.0 mol/L | |
| D. | 当V(NaOH)=4.0 L时,得到的溶液中Na+、Cl-浓度一定不相等 |
11.下列除去杂质的方法中错误的是( )
| 物质 | 杂质 | 除杂质的方法 | |
| A | SiO2 | CaCO3 | 过量稀硫酸、过滤 |
| B | 铜粉 | 铝粉 | 过量CuCl2溶液、过滤 |
| C | FeCl3溶液 | FeCl2 | 通入适量氯气 |
| D | SO2 | HC1 | 通过NaHSO3溶液的洗气瓶 |
| A. | A | B. | B | C. | C | D. | D |
10.下列实验用来证明SO2的存在,其中正确的是( )
| A. | 能使品红褪色 | |
| B. | 能使湿润的蓝色石蕊试纸变红 | |
| C. | 通入足量的NaOH溶液中,再滴入BaCl2溶液有白色沉淀生成,该沉淀溶于稀盐酸 | |
| D. | 通入稀溴水中能使溴水褪色,得澄清溶液,再滴加Ba(NO3)2溶液有白色沉淀,该沉淀不溶于硝酸 |
9.用稀H2SO4、NaOH和Al为原料制取Al(OH)3,有下列三种不同的途径,若制取等量的Al(OH)3则( )
甲:Al$\stackrel{H_{2}SO_{4}}{→}$Al2(SO4)2$\stackrel{NaOH}{→}$Al(OH)3
乙:Al$\stackrel{NaOH}{→}$NaAlO2$\stackrel{H_{2}SO_{4}}{→}$Al(OH)3
丙: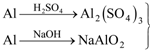 →Al(OH)3.
→Al(OH)3.
甲:Al$\stackrel{H_{2}SO_{4}}{→}$Al2(SO4)2$\stackrel{NaOH}{→}$Al(OH)3
乙:Al$\stackrel{NaOH}{→}$NaAlO2$\stackrel{H_{2}SO_{4}}{→}$Al(OH)3
丙:
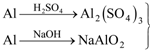 →Al(OH)3.
→Al(OH)3.| A. | 甲、乙消耗的原料同样多 | B. | 乙消耗的原料最少 | ||
| C. | 丙消耗的原料最少 | D. | 三者消耗的原料同样多 |
8.下列物质中不能由单质直接化合生成的是( )
①CuS ②FeS ③SO3 ④Fe2O3 ⑤FeCl2⑥Hg2S.
①CuS ②FeS ③SO3 ④Fe2O3 ⑤FeCl2⑥Hg2S.
| A. | ①②③⑤ | B. | ①③⑤⑥ | C. | ①③④⑤⑥ | D. | .全部 |
6.下列四种工业生产:①用海水为原料制镁;②冶炼生铁;③制漂白粉;④工业制备普通玻璃.要用石灰石作为一种原料的( )
0 171233 171241 171247 171251 171257 171259 171263 171269 171271 171277 171283 171287 171289 171293 171299 171301 171307 171311 171313 171317 171319 171323 171325 171327 171328 171329 171331 171332 171333 171335 171337 171341 171343 171347 171349 171353 171359 171361 171367 171371 171373 171377 171383 171389 171391 171397 171401 171403 171409 171413 171419 171427 203614
| A. | 只有① | B. | 只有①②③ | C. | 只有②③ | D. | 全部 |