17.磷酸铁锂(LiFePO4)电池是可循环使用的二次电池,其循环寿命是铅蓄电池的4-7倍,并有大容量、无记忆效应等优点,可用于电动汽车.该电池的正极材料是LiFePO4,负极材料是锂,电池反应为:LiFePO4$?_{放电}^{充电}$ FePO4+Li,使用含Li+导电固体为电解质.下列有关LiFePO4电池说法正确的是( )
| A. | 可加入硫酸、氢氧化钾等强电解质以提高电解质的导电性 | |
| B. | 放电时电池内部Li+向负极移动 | |
| C. | 放电过程中,电池正极材料的质量不变 | |
| D. | 放电时电池正极反应为:FePO4+Li++e-═LiFePO4 |
16.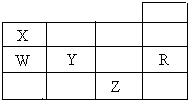 如表为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是( )
如表为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是( )
 如表为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是( )
如表为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是( )| A. | X、Y、Z的阴离子电子层结构均与R原子的相同 | |
| B. | 常压下,Y单质的沸点比Z单质的沸点高 | |
| C. | W的氢化物的稳定性比X的氢化物的稳定性强 | |
| D. | 最高价氧化物的水化物酸性W比Y强 |
15.下列关于化学反应与能量变化的关系说法正确的是( )
| A. | 由氢气燃烧放热可知,2mol氢气的能量高于2mol水的能量 | |
| B. | 燃烧天然气做饭时,其能量转化形式只有化学能转化为热能 | |
| C. | 已知碳酸钙分解为吸热反应,则CaO与CO2反应为放热反应 | |
| D. | 根据能量守恒定律分析钠在氯气中燃烧的反应可知,参与反应的钠与氯气的总能量等于生成的氯化钠的总能量 |
14.下列属于放热反应的是( )
| A. | 浓硫酸稀释 | B. | 氢气还原氧化铜 | ||
| C. | 氢氧化钡与氯化铵固体混合搅拌 | D. | 铝和稀硫酸反应 |
13.已知25%的A溶液的密度为ρ1,5%的A溶液的密度为ρ2,若将上述两种溶液等体积混合后,所得A溶液的质量分数小于15%,则下列关于ρ1和ρ2关系的表达正确的是( )
| A. | ρ1<ρ2 | B. | ρ1=ρ2 | C. | ρ1>ρ2 | D. | 无法估算 |
12.如图是硫酸试剂瓶标签上的部分内容.据此下列说法中,正确的是( )
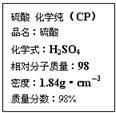

| A. | 配制200 mL 4.6 mol/L的稀硫酸需取该硫酸50 mL | |
| B. | 1 mol Zn与足量的该硫酸反应产生2 g H2 | |
| C. | 该硫酸可以用来干燥硫化氢气体 | |
| D. | 若不小心将该硫酸溅到皮肤上,应立即用NaOH溶液冲洗 |
10.近年以来,我国多地频现种种极端天气,二氧化碳、氮氧化物、二氧化硫是导致极端天气的重要因素.
(1)活性炭可用于处理大气污染物NO,在1L恒容密闭容器中加入0.100mol NO和2.030mol固体活性炭(无杂质),生成气体E和气体F.当温度分别在T1℃和T2℃时,测得平衡时各物质的物质的量如下表:
①请结合上表数据,写出NO与活性炭反应的化学方程式C+2NO?N2+CO2.
②上述反应的平衡常数表达式K=$\frac{c(N{\;}_{2})c(CO{\;}_{2})}{c(NO){\;}^{2}}$,根据上述信息判断,T1和T2的关系是C.
A.T1>T2B.T1<T2C.无法比较
③在T1℃下反应达到平衡后,下列措施能改变NO的转化率的是cd.
a.增大c(NO) b.增大压强 c.升高温度 d.移去部分F
(2)碘循环工艺不仅能吸收SO2降低环境污染,同时又能制得H2,具体流程如图1所示
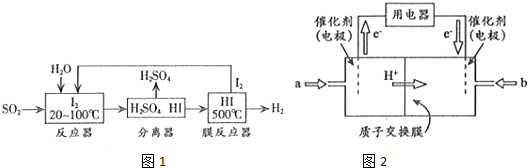
①用离子方程式表示反应器中发生的反应:SO2+I2+2H2O=SO42-+2I-+4H+.
②用化学平衡移动的原理分析,在HI分解反应中使用膜反应器分离出H2的目的是HI分解为可逆反应,及时分离出产物H2,有利于反应正向进行.
(3)开发新能源是解决大气污染的有效途径之一.直接甲醇燃料电池(简称DMFC)由于结构简单、能量转化率高、对环境无污染,可作为常规能源的替代品而越来越受到关注.DMFC工作原理如图2所示
通过a气体的电极是原电池的负极(填“正”或“负”),b电极反应式为O2+4e-+4H+=2H2O.
(1)活性炭可用于处理大气污染物NO,在1L恒容密闭容器中加入0.100mol NO和2.030mol固体活性炭(无杂质),生成气体E和气体F.当温度分别在T1℃和T2℃时,测得平衡时各物质的物质的量如下表:
 | 活性炭 | NO | E | F |
| T1 | 2.000 | 0.040 | 0.030 | 0.030 |
| T2 | 2.005 | 0.050 | 0.025 | 0.025 |
②上述反应的平衡常数表达式K=$\frac{c(N{\;}_{2})c(CO{\;}_{2})}{c(NO){\;}^{2}}$,根据上述信息判断,T1和T2的关系是C.
A.T1>T2B.T1<T2C.无法比较
③在T1℃下反应达到平衡后,下列措施能改变NO的转化率的是cd.
a.增大c(NO) b.增大压强 c.升高温度 d.移去部分F
(2)碘循环工艺不仅能吸收SO2降低环境污染,同时又能制得H2,具体流程如图1所示

①用离子方程式表示反应器中发生的反应:SO2+I2+2H2O=SO42-+2I-+4H+.
②用化学平衡移动的原理分析,在HI分解反应中使用膜反应器分离出H2的目的是HI分解为可逆反应,及时分离出产物H2,有利于反应正向进行.
(3)开发新能源是解决大气污染的有效途径之一.直接甲醇燃料电池(简称DMFC)由于结构简单、能量转化率高、对环境无污染,可作为常规能源的替代品而越来越受到关注.DMFC工作原理如图2所示
通过a气体的电极是原电池的负极(填“正”或“负”),b电极反应式为O2+4e-+4H+=2H2O.
9.如图是关于N2+3H2?2NH3(正反应为放热反应)的速率一时问图象,则t1时刻使平衡发生移动的原因是( )

| A. | 升高温度,同时增大压强 | |
| B. | 降低温度.同时减小压强 | |
| C. | 增大反应物的浓度,同时使用适宜的催化剂 | |
| D. | 增大反应物的浓度,同时减小生成物的浓度 |
8.在硫化钠水溶液中存在着多种离子和分子,下列关系式正确的是( )
0 170898 170906 170912 170916 170922 170924 170928 170934 170936 170942 170948 170952 170954 170958 170964 170966 170972 170976 170978 170982 170984 170988 170990 170992 170993 170994 170996 170997 170998 171000 171002 171006 171008 171012 171014 171018 171024 171026 171032 171036 171038 171042 171048 171054 171056 171062 171066 171068 171074 171078 171084 171092 203614
| A. | c(S2-)+c(HS-)+c(H2S)+c(H+)=c(OH-) | B. | c(OH-)=c(HS-)+c(H+)+2 c(H2S) | ||
| C. | c(Na+)=c(S2-)+c(HS-)+c(H2S) | D. | c(Na+)+c(H+)=c(S2-)+c(HS-)+c(OH-) |