题目内容
10.近年以来,我国多地频现种种极端天气,二氧化碳、氮氧化物、二氧化硫是导致极端天气的重要因素.(1)活性炭可用于处理大气污染物NO,在1L恒容密闭容器中加入0.100mol NO和2.030mol固体活性炭(无杂质),生成气体E和气体F.当温度分别在T1℃和T2℃时,测得平衡时各物质的物质的量如下表:
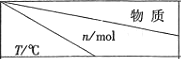 | 活性炭 | NO | E | F |
| T1 | 2.000 | 0.040 | 0.030 | 0.030 |
| T2 | 2.005 | 0.050 | 0.025 | 0.025 |
②上述反应的平衡常数表达式K=$\frac{c(N{\;}_{2})c(CO{\;}_{2})}{c(NO){\;}^{2}}$,根据上述信息判断,T1和T2的关系是C.
A.T1>T2B.T1<T2C.无法比较
③在T1℃下反应达到平衡后,下列措施能改变NO的转化率的是cd.
a.增大c(NO) b.增大压强 c.升高温度 d.移去部分F
(2)碘循环工艺不仅能吸收SO2降低环境污染,同时又能制得H2,具体流程如图1所示
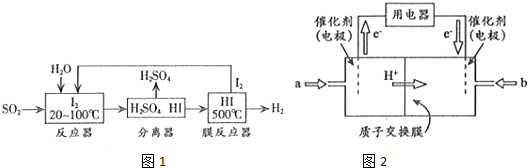
①用离子方程式表示反应器中发生的反应:SO2+I2+2H2O=SO42-+2I-+4H+.
②用化学平衡移动的原理分析,在HI分解反应中使用膜反应器分离出H2的目的是HI分解为可逆反应,及时分离出产物H2,有利于反应正向进行.
(3)开发新能源是解决大气污染的有效途径之一.直接甲醇燃料电池(简称DMFC)由于结构简单、能量转化率高、对环境无污染,可作为常规能源的替代品而越来越受到关注.DMFC工作原理如图2所示
通过a气体的电极是原电池的负极(填“正”或“负”),b电极反应式为O2+4e-+4H+=2H2O.
分析 (1)①由表中数据可知,C、NO、E、F的化学计量数之比为0.03:0.06:0.03:0.03=1:2:1:1,反应中C被氧化,结合原子守恒可知,生成为N2与CO2;
②计算各气体的平衡浓度,代入平衡常数表达式计算;由表中数据可知,温度由T1变为T2,平衡向逆反应移动,由于正反应是吸热,还是放热不确定,不能判断温度变化;
③根据平衡移动原理分析解答,
a.增大c(NO),相当于增大压强,该反应前后气体的物质的量不变,平衡不移动;
b.该反应前后气体的物质的量不变,增大压强,平衡不移动;
c.反应移动存在热效应,升高温度,平衡一定移动;
d.移去部分生成物F,平衡向正反应移动;
(2)①反应器中二氧化硫、碘发生氧化还原反应生成硫酸和HI;
②HI分解反应为可逆反应;
(3)根据图知,交换膜是质子交换膜,则电解质溶液呈酸性,根据氢离子移动方向知,通入a的电极为负极、通入b的电极为正极,负极上甲醇失去电子发生氧化反应.
解答 解:(1)①由表中数据可知,C、NO、E、F的化学计量数之比为0.03:0.06:0.03:0.03=1:2:1:1,反应中C被氧化,结合原子守恒可知,生成为N2与CO2,且该反应为可逆反应,故反应方程式为:C+2NO?N2+CO2,
故答案为:C+2NO?N2+CO2;
②从C+2NO?N2+CO2,则该反应的平衡常数表达式为K=$\frac{c(N{\;}_{2})c(CO{\;}_{2})}{c(NO){\;}^{2}}$,由表中数据可知,温度由T1变为T2,平衡向逆反应移动,由于正反应是吸热,还是放热不确定,无法判断温度变化,故答案为:$\frac{c(N{\;}_{2})c(CO{\;}_{2})}{c(NO){\;}^{2}}$;C;
③a.增大c(NO),相当于增大压强,该反应前后气体的物质的量不变,平衡不移动,NO的转化率不变,故a错误;
b.该反应前后气体的物质的量不变,增大压强,平衡不移动,NO的转化率不变,故b错误;
c.反应移动存在热效应,升高温度,平衡一定移动,NO转化率一定变化,故c正确;
d.移去部分生成物F,平衡向正反应移动,NO的转化率增大,故d正确;
故答案为:cd;
(2)①反应器中二氧化硫、碘发生氧化还原反应生成硫酸和HI,离子反应为SO2+I2+2H2O=SO42-+2I-+4H+,故答案为:SO2+I2+2H2O=SO42-+2I-+4H+;
②HI分解反应为可逆反应,则使用膜反应器分离出H2的目的是及时分离出产物H2,有利于反应正向进行,故答案为:HI分解为可逆反应,及时分离出产物H2,有利于反应正向进行;
(3)根据图知,交换膜是质子交换膜,则电解质溶液呈酸性,根据氢离子移动方向知,通入a的电极为负极、通入b的电极为正极,负极上甲醇失去电子发生氧化反应,负极反应式为 CH3OH-6e-+H2O=CO2+6H+,正极上氧气得电子发生还原反应,电极反应式为O2+4e-+4H+=2H2O,
故答案为:负;O2+4e-+4H+=2H2O.
点评 本题考查平衡常数及化学平衡的有关计算、平衡的移动以及原电池的工作原理等,难度中等,由于该反应的热效应不知,故T1和T2的关系无法比较,此为易错点.

 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案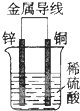
| A. | 铜片为负极 | B. | 铜片质量逐渐减少 | ||
| C. | 电子从锌片经导线流向铜片 | D. | 氢离子在铜片表面被氧化 |
| A. | 溶液中阴离子向正极移动 | |
| B. | 溶液中阴离子物质的量减少 | |
| C. | 负极的电极反应式是:N2H4+4OH--4e-═4H2O+N2↑ | |
| D. | 正极的电极反应式是:O2+4H++4e-═2H2O |
| A. | a=4 | |
| B. | 每有3 mol Fe2+参加反应,反应中转移的电子总数为5 mol | |
| C. | 将Y均匀分散到水中形成的体系具有丁达尔效应 | |
| D. | S2O32-是还原剂 |
| A. | 由氢气燃烧放热可知,2mol氢气的能量高于2mol水的能量 | |
| B. | 燃烧天然气做饭时,其能量转化形式只有化学能转化为热能 | |
| C. | 已知碳酸钙分解为吸热反应,则CaO与CO2反应为放热反应 | |
| D. | 根据能量守恒定律分析钠在氯气中燃烧的反应可知,参与反应的钠与氯气的总能量等于生成的氯化钠的总能量 |
应可表示为:5MnO2+2Ag+2NaCl═Na2Mn5O10+2AgCl 下列“水”电池在海水中放电时的有关说法正确的是( )
| A. | 正极反应式Ag+Cl--e-═AgCl | |
| B. | AgCl是还原产物 | |
| C. | Na+不断向“水”电池的负极移动 | |
| D. | 每生成1 mol Na2Mn5O10转移2 mol电子 |
| A. | 二氧化碳是造成温室效应的主要气体 | |
| B. | “白色污染”是指一些白色垃圾造成的污染 | |
| C. | 二氧化硫是形成酸雨的气体 | |
| D. | 吸烟产生的一种有毒气体是一氧化碳 |