17.在2L密闭容器内,800℃时反应:2NO(g)+O2(g)═2NO2(g),体系中,n(NO)随时间的变化如下表:
(1)该反应的平衡常数表达式为K=$\frac{{c}^{2}(N{O}_{2})}{{c}^{2}(NO)•c({O}_{2})}$;NO的平衡转化率为K=65%.
(2)0~2s内用O2来表示的化学反应速率为v(O2)=1.1×10-3mol•L-1•s-1.
(3)已知:K300℃>K350℃,则该反应是放热反应.
(4)能说明该反应已达到平衡状态的是BC.
A.v(NO2)=2v (O2) B.容器内压强保持不变 C.v(逆)(NO)=2v(正)(O2)D.容器内密度保持不变
(5)能使该反应的反应速率增大,且平衡向正反应方向移动的是C.
A.及时分离出NO2气体 B.适当升高温度 C.增大O2的浓度 D.选择高效催化剂.
| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(2)0~2s内用O2来表示的化学反应速率为v(O2)=1.1×10-3mol•L-1•s-1.
(3)已知:K300℃>K350℃,则该反应是放热反应.
(4)能说明该反应已达到平衡状态的是BC.
A.v(NO2)=2v (O2) B.容器内压强保持不变 C.v(逆)(NO)=2v(正)(O2)D.容器内密度保持不变
(5)能使该反应的反应速率增大,且平衡向正反应方向移动的是C.
A.及时分离出NO2气体 B.适当升高温度 C.增大O2的浓度 D.选择高效催化剂.
15.下列物质中,不能由单质直接化合生成的是( )
①CuS ②FeS ③SO3 ④H2S ⑤FeCl2.
①CuS ②FeS ③SO3 ④H2S ⑤FeCl2.
| A. | ①③⑤ | B. | ①②③⑤ | C. | ①②④⑤ | D. | 全部 |
11.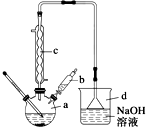 溴苯是一种常用的化工原料.实验室制备溴苯的实验步骤如下:
溴苯是一种常用的化工原料.实验室制备溴苯的实验步骤如下:
步骤1:在a中加入15mL苯和少量铁屑,再将b中4.0mL液溴慢慢加入到a中,充分反应.
步骤2:向a中加入10mL水,然后过滤除去未反应的铁屑.
步骤3:滤液依次用10mL水、8mL 10%的NaOH溶液、10mL 水洗涤,分液得粗溴苯.
步骤4:向分出的粗溴苯中加入少量的无水氯化钙,静置、过滤即得粗产品.
(1)仪器d的作用是吸收HBr防污染.
(2)将b中的液溴慢慢加入到a中,而不能快速加入的原因是防止反应放出的热使C6H6、Br2挥发而影响产率.
(3)仪器c的作用是冷凝回流,回流的主要物质有C6H6、Br2 (填化学式).
(4)步骤4得到的粗产品中还含有杂质苯.已知苯、溴苯的有关物理性质如上表,则要进一步提纯粗产品,还必须进行的实验操作名称是蒸馏.
0 170844 170852 170858 170862 170868 170870 170874 170880 170882 170888 170894 170898 170900 170904 170910 170912 170918 170922 170924 170928 170930 170934 170936 170938 170939 170940 170942 170943 170944 170946 170948 170952 170954 170958 170960 170964 170970 170972 170978 170982 170984 170988 170994 171000 171002 171008 171012 171014 171020 171024 171030 171038 203614
 溴苯是一种常用的化工原料.实验室制备溴苯的实验步骤如下:
溴苯是一种常用的化工原料.实验室制备溴苯的实验步骤如下:步骤1:在a中加入15mL苯和少量铁屑,再将b中4.0mL液溴慢慢加入到a中,充分反应.
步骤2:向a中加入10mL水,然后过滤除去未反应的铁屑.
步骤3:滤液依次用10mL水、8mL 10%的NaOH溶液、10mL 水洗涤,分液得粗溴苯.
步骤4:向分出的粗溴苯中加入少量的无水氯化钙,静置、过滤即得粗产品.
| 苯 | 溴 | 溴苯 | |
| 密度/g•cm-3 | 0.88 | 3.10 | 1.50 |
| 沸点/℃ | 80 | 59 | 156 |
| 在水中的溶解度 | 微溶 | 微溶 | 微溶 |
(2)将b中的液溴慢慢加入到a中,而不能快速加入的原因是防止反应放出的热使C6H6、Br2挥发而影响产率.
(3)仪器c的作用是冷凝回流,回流的主要物质有C6H6、Br2 (填化学式).
(4)步骤4得到的粗产品中还含有杂质苯.已知苯、溴苯的有关物理性质如上表,则要进一步提纯粗产品,还必须进行的实验操作名称是蒸馏.


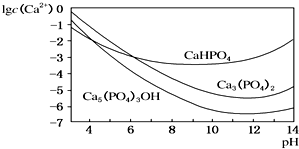 羟基磷灰石是一种重要的生物无机材料,其常用的制备方法有两种:
羟基磷灰石是一种重要的生物无机材料,其常用的制备方法有两种: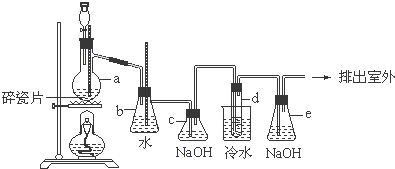
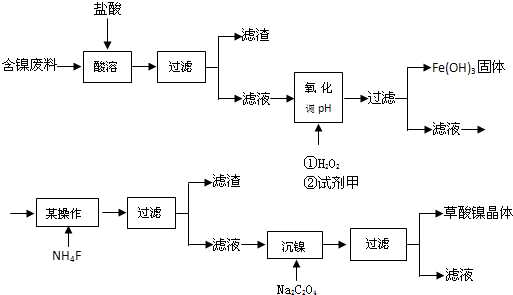
 .
.