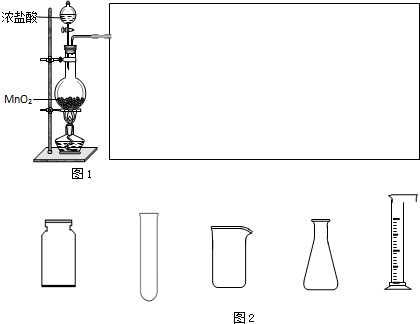
5.硼酸(H3BO3)大量应用于玻璃制造行业,以硼镁矿(2MgO•B2O3•H2O、SiO2及少量Fe3O4、CaCO3,Al2O3)为原料生产硼酸的工艺流程如图1:

已知:H3BO3在20℃、40℃、60℃、100℃时的溶解度依次为5.0g、8.7g、14.8g、40.2g.Fe3+、Al3 +、Fe2+和Mg2 +以氢氧化物形式完全沉淀时,溶液的pH分别为3.2、5.2、9.7和 12.4.
(1)由于矿粉中含CaCO3,为防止“浸取”时容易产生大量泡沫使物料从反应器中溢出,应采取的措施是:分批慢慢加入稀硫酸.
(2)“浸出液”显酸性,含H3BO3和Mg2+和SO42-,还含有Fe2+、Fe3+、Ca2+、Al3+等杂质.“除杂”时向浸出液中依次加入适量H2O2和MgO,除去的杂质离子是Fe3+、Fe2+、Al3+.H2O2的作用是H2O2+2H++2Fe2+=2Fe3++2H2O (用离子方程式表示).
(3)“浸取”后,采用“热过滤”的目的是防止温度下降时H3BO3从溶液中析出.
(4)“母液”可用于回收硫酸镁,已知硫酸镁的溶解度随温度变化的曲线如图2,且溶液的沸点随压强增大而升高.为了从“母液”中充分回收MgSO4•H20,应采取的 措施是将“母液”蒸发浓缩,加压升温结晶
(5)已知298K时,硼酸(H3BO3)溶液中存在如下反应:H3BO3(aq)+H2O(l)?[B(OH)4]-(aq)+H+(aq) K=5.7×10-10
下列说法正确的是BD.
A.碳酸钠溶液滴入硼酸中能观察到有气泡产生
B.碳酸钠溶液滴入醋酸中能观察到有气泡产生
C.等浓度的碳酸和硼酸溶液比较,pH:前者>后者
D.等浓度的碳酸钠和醋酸钠溶液比较,pH:前者>后者.

已知:H3BO3在20℃、40℃、60℃、100℃时的溶解度依次为5.0g、8.7g、14.8g、40.2g.Fe3+、Al3 +、Fe2+和Mg2 +以氢氧化物形式完全沉淀时,溶液的pH分别为3.2、5.2、9.7和 12.4.
(1)由于矿粉中含CaCO3,为防止“浸取”时容易产生大量泡沫使物料从反应器中溢出,应采取的措施是:分批慢慢加入稀硫酸.
(2)“浸出液”显酸性,含H3BO3和Mg2+和SO42-,还含有Fe2+、Fe3+、Ca2+、Al3+等杂质.“除杂”时向浸出液中依次加入适量H2O2和MgO,除去的杂质离子是Fe3+、Fe2+、Al3+.H2O2的作用是H2O2+2H++2Fe2+=2Fe3++2H2O (用离子方程式表示).
(3)“浸取”后,采用“热过滤”的目的是防止温度下降时H3BO3从溶液中析出.
(4)“母液”可用于回收硫酸镁,已知硫酸镁的溶解度随温度变化的曲线如图2,且溶液的沸点随压强增大而升高.为了从“母液”中充分回收MgSO4•H20,应采取的 措施是将“母液”蒸发浓缩,加压升温结晶
(5)已知298K时,硼酸(H3BO3)溶液中存在如下反应:H3BO3(aq)+H2O(l)?[B(OH)4]-(aq)+H+(aq) K=5.7×10-10
| 化学式 | 碳酸 | 醋酸 |
| 电离常数 | K1=4.4×10-7K2=4.7×10-11 | K=1.75×10-5 |
A.碳酸钠溶液滴入硼酸中能观察到有气泡产生
B.碳酸钠溶液滴入醋酸中能观察到有气泡产生
C.等浓度的碳酸和硼酸溶液比较,pH:前者>后者
D.等浓度的碳酸钠和醋酸钠溶液比较,pH:前者>后者.
2.据报道,有一种叫Thibacillus Ferroxidans的细菌在氧气存在下的酸性溶液中,能将黄铜矿(CuFeS2)氧化成硫酸盐.发生的反应为:4CuFeS2+2H2SO4+17O2=4CuSO4+2Fe2(SO4)3+2H2O
(1)CuFeS2中Fe的化合价为+2,上述反应中被氧化的元素是Fe和CuFeS2中的S.
(2)工业生产中利用上述反应后的溶液,按如图甲流程可制备胆矾(CuSO4•5H2O):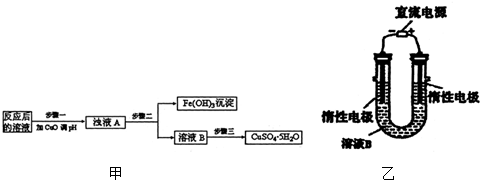
①分析表格(其中KSP是相应金属氢氧化物的沉淀溶解平衡常数):
步骤一应调节溶液的pH范围是3.2≤pH<4.7.请运用沉淀溶解平衡的有关理论解释加入CuO能除去CuSO4溶液中Fe3+的原因加入CuO与H+反应使c(H+)减小,c(OH-)增大,使溶液中c(Fe3+)•c3(OH-)>Ksp[Fe(OH)3],导致Fe3+生成沉淀而除去.
②步骤三中的具体操作方法是蒸发浓缩,冷却结晶.
(3)有人提出可以利用图乙的装置从溶液B中提炼金属铜.该过程中图乙电极的反应式是4OH--4e-=O2↑+2H2O,总反应的方程式是2CuSO4+2H2O$\frac{\underline{\;电解\;}}{\;}$2Cu+2H2SO4+O2↑.
(1)CuFeS2中Fe的化合价为+2,上述反应中被氧化的元素是Fe和CuFeS2中的S.
(2)工业生产中利用上述反应后的溶液,按如图甲流程可制备胆矾(CuSO4•5H2O):

①分析表格(其中KSP是相应金属氢氧化物的沉淀溶解平衡常数):
| Ksp | 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH | |
| Fe3+ | 2.6×10-39 | 1.9 | 3.2 |
| Cu2+ | 2.2×10-20 | 4.7 | 6.7 |
②步骤三中的具体操作方法是蒸发浓缩,冷却结晶.
(3)有人提出可以利用图乙的装置从溶液B中提炼金属铜.该过程中图乙电极的反应式是4OH--4e-=O2↑+2H2O,总反应的方程式是2CuSO4+2H2O$\frac{\underline{\;电解\;}}{\;}$2Cu+2H2SO4+O2↑.
12.萘的结构简式为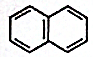 ,它与硝酸反应,可生成苯环上的一硝基取代物( )
,它与硝酸反应,可生成苯环上的一硝基取代物( )
 ,它与硝酸反应,可生成苯环上的一硝基取代物( )
,它与硝酸反应,可生成苯环上的一硝基取代物( )| A. | 1种 | B. | 2种 | C. | 3种 | D. | 4种 |
11.下列各组有机物中.肯定属于同系物的-组是( )
0 170679 170687 170693 170697 170703 170705 170709 170715 170717 170723 170729 170733 170735 170739 170745 170747 170753 170757 170759 170763 170765 170769 170771 170773 170774 170775 170777 170778 170779 170781 170783 170787 170789 170793 170795 170799 170805 170807 170813 170817 170819 170823 170829 170835 170837 170843 170847 170849 170855 170859 170865 170873 203614
| A. | C3H8 C5H12 | B. | C4H6 C3H4 | C. | C2H60 C3H8O | D. | C3H6O C2H4O |
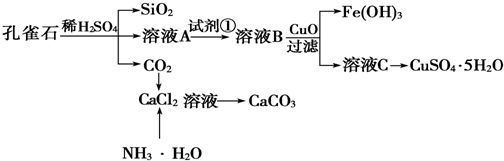
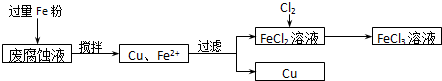
 .
.