题目内容
13.现在,科学家正在探索“反物质”,“反物质”是由“反粒子”构成的,“反粒子”与其对应的“正粒子”具有相同的质量与相同的电量,但电性相反.已知α粒子是质量数为4,带2个单位正电荷的氦原子核,据此回答:若存在反α粒子,它的质量数为4,电荷为-2.分析 根据α粒子是质量数为4,带2个单位正电荷的氦原子核,而“反粒子”与其对应的“正粒子”具有相同的质量与相同的电量,但电性相反来解答.
解答 解:α粒子是质量数为4,带2个单位正电荷,所以反α粒子,它的质量数为4,电荷为-2;
故答案为:4,-2.
点评 本题考查反粒子的特性,根据题目信息是解题的关键,比较简单.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
3.下列指定反应的离子方程式正确的是( )
| A. | 氯气溶于水:Cl2+H2O═2H++Cl-+ClO- | |
| B. | Na2CO3溶液中CO32-的水解:CO32-+H2O═HCO3-+OH- | |
| C. | 用CuSO4溶液吸收H2S气体:Cu2++S2-═CuS↓ | |
| D. | 向NaOH溶液中通入过量的CO2气体:CO2+OH-═HCO3- |
10.稀土元素是周期表中第ⅢB族钪、钇和镧系元素的总称,它们都是很活泼的金属,性质极为相似,常见化合价为+3.其中钇(Y)元素是激光和超导的重要材料.我国蕴藏着丰富的钇石矿(Y2FeBe2Si2O10),以此矿石为原料生产氧化钇(Y2O3)的主要流程如下:
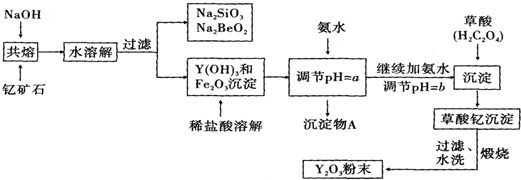
已知:①有关金属离子形成氢氧化物沉淀时的pH如下表:
②在元素周期表中,铍和铝位于第二周期和第三周期的对角线位置,化学性质相似.
(1)钇石矿(Y2FeBe2Si2O10)的组成用氧化物的形式表示为Y2O3•FeO•2BeO•2SiO2
(2)欲从Na2SiO3和Na2BeO2的混合液中制得Be(OH)2沉淀.则
①最好选用盐酸、b(填字母)两种试剂,再经过必要的操作即可实现.
a.NaOH溶液 b.氨水 c.CO2气体 d.HNO3
②写出Na2BeO2与足量盐酸发生反应的离子方程式:BeO22-+4H+=Be2++2H2O
(3)上述过程中用氨水调节pH=a的目的是使Fe3+完全水解形成沉淀而除去,a应控制在3.7~6.0范围内;写出生成沉淀物A的离子方程式Fe3++3NH3•H2O=Fe(OH)3↓+3NH4+,检验该过程是否沉淀完全的操作方法是取少量滤液,滴加几滴KSCN溶液,观察溶液是否变为血红色,若不变血红色,则说明Fe3+完全沉淀,反之则未完全沉淀.
(4)写出由草酸钇沉淀制备氧化钇的化学方程式Y2(C2O4)3$\frac{\underline{\;高温\;}}{\;}$Y2O3+3CO↑+3CO2↑.

已知:①有关金属离子形成氢氧化物沉淀时的pH如下表:
| 开始沉淀时的pH | 完全沉淀时的pH | |
| Fe3+ | 2.7 | 3.7 |
| Y3+ | 6.0 | 8.2 |
(1)钇石矿(Y2FeBe2Si2O10)的组成用氧化物的形式表示为Y2O3•FeO•2BeO•2SiO2
(2)欲从Na2SiO3和Na2BeO2的混合液中制得Be(OH)2沉淀.则
①最好选用盐酸、b(填字母)两种试剂,再经过必要的操作即可实现.
a.NaOH溶液 b.氨水 c.CO2气体 d.HNO3
②写出Na2BeO2与足量盐酸发生反应的离子方程式:BeO22-+4H+=Be2++2H2O
(3)上述过程中用氨水调节pH=a的目的是使Fe3+完全水解形成沉淀而除去,a应控制在3.7~6.0范围内;写出生成沉淀物A的离子方程式Fe3++3NH3•H2O=Fe(OH)3↓+3NH4+,检验该过程是否沉淀完全的操作方法是取少量滤液,滴加几滴KSCN溶液,观察溶液是否变为血红色,若不变血红色,则说明Fe3+完全沉淀,反之则未完全沉淀.
(4)写出由草酸钇沉淀制备氧化钇的化学方程式Y2(C2O4)3$\frac{\underline{\;高温\;}}{\;}$Y2O3+3CO↑+3CO2↑.
7.下列有关化学用语表示正确的是( )
| A. | 乙烯的结构简式:CH2CH2 | B. | 乙酸的结构式:CH3COOH | ||
| C. | 2-丁烯的键线式: | D. | 乙醇分子的比例模型: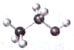 |
8.25℃,向20mL 0.1mol•L-1的H3PO2溶液中滴加0.1mol•L-1的NaOH溶液(滴定过程中溶液温度保持不变),滴定曲线如图1,含磷物种浓度所占分数(δ)随pH变化关系如图2,则下列说法不正确的是( )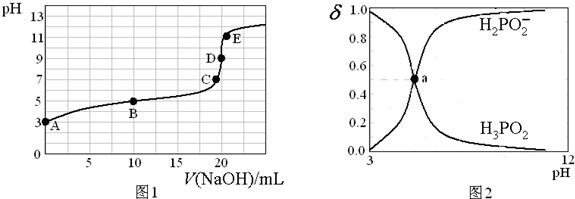

| A. | H3PO2的电离方程式为:H3PO2?H2PO2-+H+;电离常数Ka≈10-5 | |
| B. | B点溶液中存在关系:2c(H+)+c(H3PO2)=2c(OH-)+c(H2PO2-) | |
| C. | 图2中的a点对应为 图1中的B点 | |
| D. | D点时,溶液中微粒浓度大小关系为:c(Na+)>c(H2PO2-)>c(OH-)>c(H+) |