3.NA表示阿伏德罗常数的额值,下列说法正确的是( )

| A. | 5.6g铁粉在0.1mol氯气中充分燃烧,转移电子数为0.3NA | |
| B. | 12.5mL 16mol•L-1浓硫酸与足量铜反应,转移电子数为0.2NA | |
| C. | 7.8g Na2S和Na2O2的混合物中含有的阴离子数等于0.1NA | |
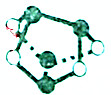
| D. | 0.5mol雄黄(As4S4,结构如图),含有NA个As-S键 |
2.下列由实验现象不能得出正确结论的是( )
| 选项 | 实验现象 | 结论 |
| A | 把相同大小的一块铝和镁分别投入相同浓度的盐酸中,镁溶解有气泡产生,而铝没有任何变化 | 镁的金属性比铝强 |
| B | 取一块铝箔,用酒精灯点燃,铝箔只熔化成液体 | 铝不易燃烧 |
| C | 向氯化铵溶液中投入一铝片,铝上产生大量气泡 | 该气体是氢气 |
| D | 向氯化铝溶液中逐滴滴加NaOH溶液至过量,先产生沉淀,后沉淀逐渐溶解,最后沉淀完全消失 | 氢氧化铝能溶解于强碱溶液 |
| A. | A | B. | B | C. | C | D. | D |
1.下列离子方程式书写正确的是( )
| A. | 氢氧化镁中滴加盐酸:H++OH-═H2O | |
| B. | 在硫酸氢钾溶液中加入氢氧化钡溶液至溶液呈中性:H++SO42-+Ba2++OH-═BaSO4↓+H2O | |
| C. | 已知电离平衡常数:H2CO3>HClO>HCO3-,向次氯酸钠溶液中通入少量二氧化碳:2ClO-+CO2+H2O═2HClO+CO32- | |
| D. | 向NH4Al(SO4)2溶液中滴入Ba(OH)2溶液,恰好使SO42-完全沉淀:NH4++Al3++2SO42-+2Ba2++4OH-═Al(OH)3↓+NH3•H2O+2BaSO4↓ |
20.下列有关铝的化合物的说法正确的是( )
| A. | 氧化铝坩埚可用于熔融NaOH实验 | |
| B. | 氧化铝的熔点很高,是一种较好的耐火材料 | |
| C. | 明矾可用于自来水的消毒 | |
| D. | 氢氧化铝能中和胃酸,适合于胃溃疡患者服用 |
19.下列叙述中正确的是( )
| A. | 1mol H2与0.5mol H2和O2的混合物所含的原子数目相同 | |
| B. | 32g O2含有6.02×1023个氧分子 | |
| C. | 1mol H2O中含有2mol H2,1mol O,总共所含电子的物质的量为10mol | |
| D. | 物质的量为1mol 的任何微粒的质量与NA个该种微粒的质量在任何情况下都相等 |
18.一定量的Al2(SO4)3,ZnSO4,Na2SO4三种溶液分别与足量BaCl2溶液反应.若生成BaSO4沉淀质量比为1:2:3,则三种硫酸盐溶液的物质的量比为( )
| A. | 1:6:9 | B. | 1:2:3 | C. | 1:3:3 | D. | 1:3:6 |
17.可选家发现了一种新型氢分子,其分子式为H3,关于原子个数相同的H3和H2,下列说法中一定正确的是( )
| A. | 体积一定相等 | B. | 分子数一定相等 | ||
| C. | 质量一定相等 | D. | 物质的量一定相等 |
16.2.16g X2O5中含有0.1mol O,则X元素为( )
| A. | Ne | B. | Si | C. | N | D. | P |
14.已知键能数据:1mol H-N:390.8kJ/mol;1mol N≡N:946kJ/mol;1mol H-H:436.0kJ/mol对反应3H2+N2═2NH3,其反应热的表述正确的是( )
0 170613 170621 170627 170631 170637 170639 170643 170649 170651 170657 170663 170667 170669 170673 170679 170681 170687 170691 170693 170697 170699 170703 170705 170707 170708 170709 170711 170712 170713 170715 170717 170721 170723 170727 170729 170733 170739 170741 170747 170751 170753 170757 170763 170769 170771 170777 170781 170783 170789 170793 170799 170807 203614
| A. | △H=-600.4kJ/mol | B. | △H=-1081.6kJ/mol | ||
| C. | △H=+90.8kJ/mol | D. | △H=-90.8kJ/mol |