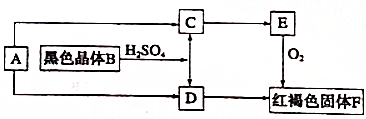
题目内容
17.可选家发现了一种新型氢分子,其分子式为H3,关于原子个数相同的H3和H2,下列说法中一定正确的是( )| A. | 体积一定相等 | B. | 分子数一定相等 | ||
| C. | 质量一定相等 | D. | 物质的量一定相等 |
分析 原子个数相同的H3和H2,可设原子的物质的量均为6mol,则H3和H2的物质的量分别为2mol、3mol,结合V=nVm、N=nNA、m=nM计算.
解答 解:原子个数相同的H3和H2,可设原子的物质的量均为6mol,则H3和H2的物质的量分别为2mol、3mol,
A.状况未知,Vm不确定,则不能比较体积,故A错误;
B.由N=nNA可知,气体的物质的量不等,则分子数不同,故B错误;
C.当原子均为6mol时,H的摩尔质量相同,则质量相同,故C正确;
D.由上述分析可知,原子物质的量相同,分子的物质的量不同,故D错误;
故选C.
点评 本题考查物质的量的计算,为高频考点,把握物质的构成及物质的量为中心的基本计算公式为解答的关键,侧重分析与计算能力的考查,题目难度不大.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
8.下列有关物质分类或归类正确的一组是
①液氨、液氯、干冰、碘化银均为化合物
②氢氟酸、盐酸、纯碱、氨水均为混合物
③明矾、小苏打、醋酸、次氯酸均为电解质
④烟、云、雾、豆浆均为胶体
⑤Na2O2、Na2CO3、NaHCO3、Na2SiO3均为钠盐
⑥NaCl、Na2CO3、NaHSO4、NaF均为正盐( )
①液氨、液氯、干冰、碘化银均为化合物
②氢氟酸、盐酸、纯碱、氨水均为混合物
③明矾、小苏打、醋酸、次氯酸均为电解质
④烟、云、雾、豆浆均为胶体
⑤Na2O2、Na2CO3、NaHCO3、Na2SiO3均为钠盐
⑥NaCl、Na2CO3、NaHSO4、NaF均为正盐( )
| A. | ①和② | B. | ②和③ | C. | ③和④ | D. | ②③⑥ |
2.下列由实验现象不能得出正确结论的是( )
| 选项 | 实验现象 | 结论 |
| A | 把相同大小的一块铝和镁分别投入相同浓度的盐酸中,镁溶解有气泡产生,而铝没有任何变化 | 镁的金属性比铝强 |
| B | 取一块铝箔,用酒精灯点燃,铝箔只熔化成液体 | 铝不易燃烧 |
| C | 向氯化铵溶液中投入一铝片,铝上产生大量气泡 | 该气体是氢气 |
| D | 向氯化铝溶液中逐滴滴加NaOH溶液至过量,先产生沉淀,后沉淀逐渐溶解,最后沉淀完全消失 | 氢氧化铝能溶解于强碱溶液 |
| A. | A | B. | B | C. | C | D. | D |
9.下列有关胶体的叙述中不正确的是( )
| A. | 溶液、胶体、浊液最本质区别是分散质粒子直径的大小 | |
| B. | “雨后彩虹”既是一种自然现象又是光学现象,同时也与胶体有关 | |
| C. | 在溶有1mol Fe(OH)3的胶体中,含有NA个Fe(OH)3胶粒 | |
| D. | 分散质粒子大小介于1~100nm之间的分散系称为胶体 |
6.室温下,在pH=13的某溶液中,由水电离出的c(OH-)为( )
①1.0×10-7mol/L②1.0×10-6mol/L③1.0×10-1mol/L④1.0×10-13mol/L.
①1.0×10-7mol/L②1.0×10-6mol/L③1.0×10-1mol/L④1.0×10-13mol/L.
| A. | ③ | B. | ③或④ | C. | ①或③ | D. | ④ |
17.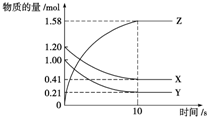 一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示.下列描述正确的是( )
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示.下列描述正确的是( )
 一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示.下列描述正确的是( )
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示.下列描述正确的是( )| A. | 反应在0~10 s内,用Z表示的反应速率为0.158 mol•L-1•s-1 | |
| B. | 反应在0~10 s内,X的物质的量浓度减少了0.79 mol•L-1 | |
| C. | 反应进行到10 s时,Y的转化率为79.0% | |
| D. | 反应的化学方程式为X(g)+Y(g)═Z(g) |