15.现有A、B、C、D、E、F六种位于周期表前四周期元素,其原子序数依次增大,相关信息如表所示:
根据以上信息,回答下列问题:
(1)画出元素C的基态价电子排布图: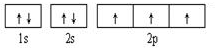 ;F元素位于周期表的d区;B、C、D三种元素的第一电离能由大到小顺序为:N>O>C(用元素符号表示).
;F元素位于周期表的d区;B、C、D三种元素的第一电离能由大到小顺序为:N>O>C(用元素符号表示).
(2)化合物BA2D2蒸气293K时,理论测算密度为2.0g•L-1,实际密度为2.5g•L-1的原因是甲酸形成分子间氢键.
(3)ED2中F原子的杂化类型为sp2; ED2易溶于水的原因可能是:①②(填入序号).
①ED2与水极性相同 ②ED2可以与水反应
(4)有人推测化合物CA5的存在,该化合物中含有化学键的可能类型为:离子键、共价键.
| 元素 | 性质 |
| A | 一种核素的原子核内不含中子 |
| B | 原子核外电子有6种不同运动状态 |
| C | 最高价氧化物的水化物与其氢化物可发生非氧化还原反应 |
| D | 单质之一为淡蓝色气体,可阻挡对人体有害的紫外线 |
| E | 周期表中位于短周期,基态原子M层成对电子数是未成对电子数的2倍 |
| F | 该元素的一种氧化物M可用作油漆颜料,与某单质反应可应用于焊接钢轨 |
(1)画出元素C的基态价电子排布图:
 ;F元素位于周期表的d区;B、C、D三种元素的第一电离能由大到小顺序为:N>O>C(用元素符号表示).
;F元素位于周期表的d区;B、C、D三种元素的第一电离能由大到小顺序为:N>O>C(用元素符号表示).(2)化合物BA2D2蒸气293K时,理论测算密度为2.0g•L-1,实际密度为2.5g•L-1的原因是甲酸形成分子间氢键.
(3)ED2中F原子的杂化类型为sp2; ED2易溶于水的原因可能是:①②(填入序号).
①ED2与水极性相同 ②ED2可以与水反应
(4)有人推测化合物CA5的存在,该化合物中含有化学键的可能类型为:离子键、共价键.
14.某溶液中含有HCO3-、SO32-、CO32-、CH3COO-四种阴离子,向其中加入过量的过氧化钠固体后,离子浓度变大的是( )
| A. | HCO3- | B. | SO32- | C. | CO32- | D. | CH3COO- |
13.下列物质中,均直接由原子构成的是:①干冰;②二氧化硅;③水蒸气;④金刚石;⑤单晶硅;⑥白磷;⑦硫磺;⑧液氨;⑨钠;⑩氖晶体( )
| A. | ②③④⑤ | B. | ②③④⑤⑨⑩ | C. | ②④⑤⑩ | D. | ②④⑤⑥⑦⑨⑩ |
12.某课外实验小组设计的下列实验不合理的是( )
| A. | 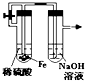 制备并观察氢氧化亚铁 | B. | 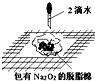 证明过氧化钠与水反应放热 | ||
| C. | 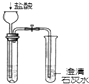 鉴别碳酸钠与亚硫酸钠 | D. | 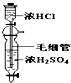 制备少量干燥的氯化氢气体 |
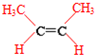
7.分子式为C3H4Cl2的同分异构体共有(含一个碳碳双键,不考虑立体异构)( )
0 170499 170507 170513 170517 170523 170525 170529 170535 170537 170543 170549 170553 170555 170559 170565 170567 170573 170577 170579 170583 170585 170589 170591 170593 170594 170595 170597 170598 170599 170601 170603 170607 170609 170613 170615 170619 170625 170627 170633 170637 170639 170643 170649 170655 170657 170663 170667 170669 170675 170679 170685 170693 203614
| A. | 5种 | B. | 6种 | C. | 7种 | D. | 8种 |
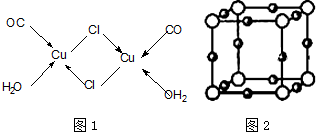

 铁和铁的化合物用途广泛.请回答下列问题:
铁和铁的化合物用途广泛.请回答下列问题: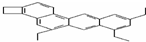 doggycene的分子式为C26H26.
doggycene的分子式为C26H26.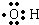 ;
; ;
;