题目内容
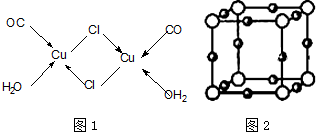
11.实现“节能减排”和“低碳经济”的一项重要课题就是如何将CO2转化为可利用的资源.目前工业上有一种方法是用CO2来生产燃料甲醇.一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g),图1表示该反应过程中能量变化:
(1)关于该反应的下列说法中,正确的是C(填字母).
A.△H>0,△S>0B.△H>0,△S<0
C.△H<0,△S<0D.△H<0,△S>0
(2)为探究反应原理,现进行如下实验,在体积为l L的密闭容器中,充入l mol CO2和4mol H2,一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如图2所示.
①从反应开始到平衡,CO2的平均反应速率v(CO2)=0.075 mol•L-1•min-1.
②该反应的平衡常数表达式K=$\frac{C(CH{\;}_{3}OH)•C(H{\;}_{2}O)}{C(CO{\;}_{2})•C{\;}^{3}(H{\;}_{2})}$.
③下列措施中能使化学平衡向正反应方向移动的是B(填字母).
A.升高温度 B.将CH3OH(g)及时液化抽出 C.选择高效催化剂
(3)25℃,1.01×105Pa时,16g 液态甲醇完全燃烧,当恢复到原状态时,放出363.3kJ的热量,写出该反应的热化学方程式:CH3OH(l)+$\frac{3}{2}$O2(g)=CO2(g)+2H2O(l)△H=-726.6 kJ•mol-1.
分析 (1)依据反应和图象分析判断:CO2(g)+3H2(g)?CH3OH(g)+H2O(g),反应是熵减少的反应△S<0;反应物能量高于生成物的能量,判断反应是放热反应,△H<0;
(2)在体积为l L的密闭容器中,充入l mol CO2和4mol H2,一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如图2所示.二氧化碳是反应物随反应进行浓度减小,甲醇是生成物,随反应进行浓度增大;10nim内达到平衡,生成甲醇浓度为0.75mol/L,二氧化碳浓度变化了0.75mol/L;
①依据化学平衡三段式列式计算判断;
②依据化学平衡常数的概念书写平衡常数计算式;
③依据化学反应的影响因素和条件逐项分析判断;
A、反应是放热反应,升温平衡逆向进行;
B、将CH3OH(g)及时液化抽出,减小生成物的量平衡正向进行;
C、选择高效催化剂只能改变速率,不改变化学平衡;
(3)25℃,1.01×105Pa时,16g 液态甲醇完全燃烧,当恢复到原状态时,放出363.3kJ的热量,依据书写热化学方程式的方法写出该反应的热化学方程式为:CH3OH(l)+$\frac{3}{2}$O2(g)=CO2(g)+2H2O(l)△H=-726.6 kJ•mol-1.
解答 解:(1)依据反应和图象分析判断:CO2(g)+3H2(g)?CH3OH(g)+H2O(g),反应是熵减少的反应△S<0;反应物能量高于生成物的能量,判断反应是放热反应,△H<0,
故答案为:C;
(2)在体积为l L的密闭容器中,充入l mol CO2和4mol H2,一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如图2所示.二氧化碳是反应物随反应进行浓度减小,甲醇是生成物,随反应进行浓度增大;10nim内达到平衡,生成甲醇浓度为0.75mol/L,二氧化碳浓度变化了0.75mol/L;则
①依据化学平衡列式计算为:
CO2(g)+3H2(g)?CH3OH(g)+H2O(g)
起始量(mol/L) 1 4 0 0
变化量(mol/L) 0.75 2.25 0.75 0.75
平衡量(mol/L) 0.25 1.75 0.75 0.75
CO2的平均反应速率v(CO2)=$\frac{0.75mol/L}{10min}$=0.075mol•L-1•min-1 ;故答案为:0.075 mol•L-1•min-1;
②该反应的平衡常数表达式K=$\frac{C(CH{\;}_{3}OH)•C(H{\;}_{2}O)}{C(CO{\;}_{2})•C{\;}^{3}(H{\;}_{2})}$,故答案为:$\frac{C(CH{\;}_{3}OH)•C(H{\;}_{2}O)}{C(CO{\;}_{2})•C{\;}^{3}(H{\;}_{2})}$;
③措施中能使化学平衡向正反应方向移动的是:
A、反应是放热反应,升温平衡逆向进行;故A错误;
B、将CH3OH(g)及时液化抽出,减小生成物的量,平衡正向进行,故B正确;
C、选择高效催化剂只能改变速率,不改变化学平衡,故C错误;
故选B;
(3)25℃,1.01×105Pa时,16g 液态甲醇物质的量为0.5mol,完全燃烧,当恢复到原状态时,放出363.3kJ的热量,依据书写热化学方程式的方法写出该反应的热化学方程式为:CH3OH(l)+$\frac{3}{2}$O2(g)=CO2(g)+2H2O(l)△H=-726.6 kJ•mol-1;
故答案为:CH3OH(l)+$\frac{3}{2}$O2(g)=CO2(g)+2H2O(l)△H=-726.6 kJ•mol-1.
点评 本题考查了反应的焓变判断,热化学方程式的书写原则,电极反应和电池反应的分析书写,化学平衡的影响因素判断平衡移动方向,化学平衡的计算的应用,图象分析是关键.综合性较大,难度中等.

| A. | 在蔗糖中加入浓硫酸后出现发黑现象,说明浓硫酸具有脱水性 | |
| B. | 浓硝酸在光照下颜色变黄,说明浓硝酸不稳定 | |
| C. | 常温下,浓硝酸可以用铝罐贮存,说明铝与浓硝酸不反应 | |
| D. | 氯水可使石蕊试液先变红后褪色,说明氯水具有酸性、漂白性 |
| A. | Ca(ClO)2溶液中通入少量SO2:Ca2++2ClO-+SO2+H2O═CaSO3↓+2HClO | |
| B. | 将Cl2通入水中:Cl2+H2O═2H++Cl-+ClO- | |
| C. | MnO2与浓盐酸共热制Cl2:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O | |
| D. | Cl2通入冷的NaOH溶液中:2Cl2+2OH-═3Cl-+ClO-+H2O |
| A. | 增大盐酸的浓度 | B. | 提高反应的温度 | C. | 用锌粉代替锌片 | D. | 用纯锌代替粗锌 |
| 选项 | 学生甲 | 学生乙 |
| A | 向碳酸氢钠溶液中逐渐加入盐酸 | 向盐酸中逐滴加入碳酸氢钠溶液 |
| B | 向氯化亚铁溶液中滴加KSCN溶液,再通入氯气 | 向氯化亚铁溶液中通入氯气,再滴加KSCN溶液 |
| C | 向FeBr2溶液中通入少量Cl2 | 向FeBr2溶液中通入足量Cl2 |
| D | 向BaCl2溶液中通入二氧化硫 | 向BaCl2溶液中通入SO3 |
| A. | A | B. | B | C. | C | D. | D |
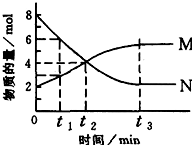 在一定温度下,某容器内某一反应中,M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )
在一定温度下,某容器内某一反应中,M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )| A. | 此反应为不可逆反应 | B. | t2时,正逆反应速率相等,达到平衡 | ||
| C. | t3时,正反应速率大于逆反应速率 | D. | t3时,正反应速率等于逆反应速率 |
| A. | 我国最早使用的合金是由铜锌合金制成的青铜器 | |
| B. | 储氢合金是一类能大量吸收H2,并与H2结合成金属氢化物的材料 | |
| C. | 一般汽车配件中的发动机使用的是密度小、强度大且耐腐蚀的铝合金材料 | |
| D. | 钛合金,形状记忆合金,耐热合金以及储氢合金都属于新型合金 |
 .
.