4.设NA 为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 1 L 0.1 mol•L-1的氨水含有0.1NA个OH- | |
| B. | 1 L 1 mol•L-1的NaClO溶液中含有ClO-的数目为NA | |
| C. | 25℃时,pH=13的Ba(OH)2溶液中含有OH-的数目为0.1 NA | |
| D. | 在电解精炼粗铜的过程中,当阴极析出32 g铜时转移电子数为NA |
3.下列叙述正确的是( )
| A. | 原子半径:Al>Mg>Na | B. | 热稳定性:NH3>PH3>H2S | ||
| C. | 酸性:HClO4>H2SiO3>H3PO4 | D. | 元素非金属性:F>O>N |
2.根据化学反应的实质--旧键的断裂和新键的形成,判断下列变化不属于化学变化的是( )
| A. | 水通电生成氢气和氧气 | B. | 金刚石在一定条件下转化为石墨 | ||
| C. | 氯化钠在水溶液中发生电离 | D. | Na2O转化为Na2O2 |
1.下列反应中属于吸热反应的是( )
| A. | 煅烧石灰石制生石灰 | B. | 燃烧木炭取暖 | ||
| C. | 硝酸与氢氧化钾反应 | D. | 钠与水反应制取氢气 |
20.研究有机物一般经过以下几个基本步骤:分离、提纯→确定实验式→确定分子式→确定结构式.有机物A可由葡萄糖发酵得到,也可从酸牛奶中提取.纯净的A为无色粘稠液体,易溶于水.为研究A的组成与结构,进行了如下实验:
| 实 验 步 骤 | 解 释 或 实 验 结 论 |
| (1)称取A 9.0g,升温使其汽化,测其密度是相同条件下H2的45倍. | 试通过计算填空:(1)A的相对分子质量为90. |
| (2)将此9.0gA在足量纯O2中充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现两者分别增重5.4g和13.2g. | (2)A的分子C3H6O3. |
| (3)另取A 9.0g,跟足量的NaHCO3粉末反应,生成2.24LCO2(标准状况),若与足量金属钠反应则生成2.24LH2(标准状况). | (3)写出A中含有的官能团的名称 羧基、羟基. |
| (4)若A中含有4种不同环境的氢原子. | 综上所述,A的结构简式为 或HOCH2CH2COOH. 或HOCH2CH2COOH. |
18.下列反应属于取代反应的是( )
| A. | 催化剂作用下,环氧丙烷和二氧化碳制备全降解塑料 | |
| B. | 催化剂作用下,乙烯和水制乙醇反应 | |
| C. | 乙醇在铜催化作用下与氧气的反应 | |
| D. | 甲烷和氯气光照条件下反应 |
17.下列说法正确的是( )
| A. | 红牛配方中有三类物质:一是B族维生素,二是人体必需的氨基酸,三是咖啡因.这些对人体都是有益无害的 | |
| B. | 淀粉和纤维素的化学式均为(C6H10O5)n,二者互为同分异构体 | |
| C. | 乙酸乙酯在碱性条件下水解叫皂化反应 | |
| D. | 蛋白质溶液具有丁达尔效应 |
16.取一定质量的下列各组物质混合后,无论以何种比例混合,其充分燃烧后一定能得到相同物质的量的二氧化碳和水的是( )
0 170388 170396 170402 170406 170412 170414 170418 170424 170426 170432 170438 170442 170444 170448 170454 170456 170462 170466 170468 170472 170474 170478 170480 170482 170483 170484 170486 170487 170488 170490 170492 170496 170498 170502 170504 170508 170514 170516 170522 170526 170528 170532 170538 170544 170546 170552 170556 170558 170564 170568 170574 170582 203614
| A. | C2H2 C2H6 | B. | CH4 C3H8 | C. | C3H6 C3H8 | D. | C2H4 C4H8 |
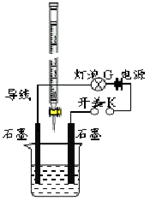 某温度下,水的离子积Kw=l×10-13.有酸溶液A,pH=a;碱溶液B,pH=b.为测定A、B混合后溶液导电性的变化以及探究A、B的相关性质,某同学设计了如图所示的实验装置.
某温度下,水的离子积Kw=l×10-13.有酸溶液A,pH=a;碱溶液B,pH=b.为测定A、B混合后溶液导电性的变化以及探究A、B的相关性质,某同学设计了如图所示的实验装置.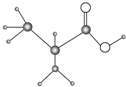 如图是只含有C、H、O、N四种元素的有机物的简易球棍模型,完成下列问题:
如图是只含有C、H、O、N四种元素的有机物的简易球棍模型,完成下列问题: .
.