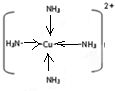
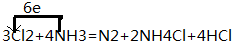20.某元素质量数51,中子数27,其基态原子未成对电子数为( )
| A. | 3 | B. | 4 | C. | 5 | D. | 6 |
19.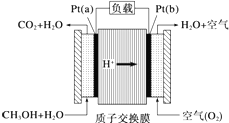 科学家预言,燃料电池将是 21世纪获得电能的重要途径.近几年开发的甲醇燃料电池是采用铂作电极,电池中的质子交换膜只允许 H+ 和水分子通过.其工作原理的示意图如下.下列说法错误的是( )
科学家预言,燃料电池将是 21世纪获得电能的重要途径.近几年开发的甲醇燃料电池是采用铂作电极,电池中的质子交换膜只允许 H+ 和水分子通过.其工作原理的示意图如下.下列说法错误的是( )
 科学家预言,燃料电池将是 21世纪获得电能的重要途径.近几年开发的甲醇燃料电池是采用铂作电极,电池中的质子交换膜只允许 H+ 和水分子通过.其工作原理的示意图如下.下列说法错误的是( )
科学家预言,燃料电池将是 21世纪获得电能的重要途径.近几年开发的甲醇燃料电池是采用铂作电极,电池中的质子交换膜只允许 H+ 和水分子通过.其工作原理的示意图如下.下列说法错误的是( )| A. | a 是负极,b 是正极 | |
| B. | b 极的电极反应是 O2+4H++4e-═2H2O | |
| C. | 放电过程中,电子流动方向为:a→b→质子交换膜→a | |
| D. | 当电路上通过 2 mol 电子消耗的 CH3OH 为 $\frac{1}{3}$mol |
18.下列叙述正确的是( )
| A. | 24Mg32S 晶体中电子总数与中子总数之比为 1:1 | |
| B. | CO2和 PCl5分子中各原子最外层都满足 8 电子结构 | |
| C. | 若 aXm+ 和 bYn- 两种离子电子层结构相同,则 a-b=n-m | |
| D. | 元素周期表中第 4 列元素形成的化合物数目最多 |
17.铅蓄电池的两极分别是 Pb、PbO2,电解质溶液为 30%硫酸,工作时反应为:Pb+PbO2+2H2SO4$?_{充电}^{放电}$2PbSO4+2H2O,该电池放电时,下列结论正确的是( )
| A. | PbO2 为正极,被氧化 | |
| B. | 电解质溶液中 c(H+) 逐渐增大 | |
| C. | 电池电解质溶液的密度不断减小 | |
| D. | 该电池的负极反应式为:Pb-2e-═Pb2+ |
16.下列说法正确的是( )
| A. | 铝热反应属于氧化还原反应,且生成物的总能量高于反应物的总能量 | |
| B. | 在相同温度和压强下,等质量的硫在足量的纯氧中燃烧放出能量为 Q1,在空气中燃烧放出能量为 Q2,则 Q1=Q2 | |
| C. | 需要加热的反应一定是吸热反应 | |
| D. | 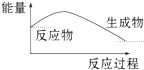 Ba(OH)2•8H2O 晶体和 NH4Cl 晶体反应能量变化如图所示 |
14.下列离子方程式,一定正确的是( )
| A. | 硫化亚铁与稀硝酸反应:FeS+2H+→Fe2++H2S | |
| B. | 纯碱溶液中滴加少量盐酸:CO32-+H+→HCO3- | |
| C. | 过量的NaHSO4与Ba(OH)2溶液反应:Ba2++2OH-+2H++SO42-→BaSO4↓+2H2O | |
| D. | 将少量SO2气体通入Ca(ClO)2溶液中:SO2+Ca2++2ClO-+H2O→CaSO3↓+2HClO |
13.下列各组离子能在指定溶液中大量共存的是( )
0 170035 170043 170049 170053 170059 170061 170065 170071 170073 170079 170085 170089 170091 170095 170101 170103 170109 170113 170115 170119 170121 170125 170127 170129 170130 170131 170133 170134 170135 170137 170139 170143 170145 170149 170151 170155 170161 170163 170169 170173 170175 170179 170185 170191 170193 170199 170203 170205 170211 170215 170221 170229 203614
| A. | 在能使石蕊试纸变蓝色的溶液中:Na+、SO32ˉ、S2ˉ、SO42ˉ | |
| B. | 由水电离的H+浓度c(H+)=10-12mol•L-1的溶液中:Clˉ、CO32ˉ、NH4+、NO3ˉ | |
| C. | 在加入铝粉能产生H2的溶液中:NH4+、Na+、Fe2+、NO3ˉ | |
| D. | pH=2的溶液中:Na+、SO42ˉ、NO3ˉ、AlO2ˉ |