9.下列物质之间的相互关系错误的是( )
| A. | H和D互为同位素 | B. | 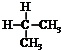 与 与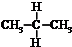 互为同分异构体 互为同分异构体 | ||
| C. | CH3CH3和CH3CH2CH3互为同系物 | D. | O2和O3互为同素异形体 |
8.下面有机物的同系物中,完全燃烧产生的水和二氧化碳的物质的量之比恒定的是①饱和一元醇②饱和一元醛③饱和一元羧酸④饱和一元醇和饱和一元羧酸生成的酯⑤乙炔的同系物⑥苯的同系物( )
| A. | ①④ | B. | ②③④⑤⑥ | C. | ②③ | D. | ②③④ |
7.下列每组中各有三对物质,它们都能用分液漏斗分离的是( )
| A. | 甘油和水、乙醛和水、乙酸和乙醇 | |
| B. | 油酸和水、甲苯和水、己烷和苯 | |
| C. | 乙酸乙酯和水、酒精和水、苯酚和水 | |
| D. | 二溴乙烷和水、溴苯和水、硝基苯和水 |
5.除去下列物质中含有的少量杂质(括号内为杂质)方法正确的是( )
| A. | C2H6(C2H4),用镍做催化剂共热. | |
| B. | C2H4(SO2),通过盛氯水溶液洗气瓶,再用碱石灰干燥 | |
| C. | 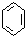 ( (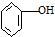 )加入过量浓溴水,先过滤;再分液 )加入过量浓溴水,先过滤;再分液 | |
| D. | C2H5Br(C2H5OH)先用大量水洗涤,然后分液 |
4.短周期元素X、Y、Z、M、N原子序数依次增大,有关信息如下:
请回答:
(1)X2Z的电子式是 ;M2Z中所含化学键类型是离子键.
;M2Z中所含化学键类型是离子键.
(2)Y的非金属性比N强(填“强”或“弱”),能证明此结论的事实是CO 2+H 2O+SiO32-=H 2SiO 3↓+CO 32-(用离子方程式表示).
(3)YX4的结构简式为CH4;分子里各原子的空间分布具有正四面体结构;在光照的条件下,将1mol YX4与1mol Cl2混合充分反应后,得到的产物最多有5种.
| 元素 | 有关信息 |
| X | 在元素周期表中原子半径最小 |
| Y | 最外层电子数是次外层的2倍 |
| Z | 元素的主要合价为一2价 |
| M | 其单质及化合物的焰色反应呈黄色 |
| N | 与Y同主族,其单质为半导体 |
(1)X2Z的电子式是
 ;M2Z中所含化学键类型是离子键.
;M2Z中所含化学键类型是离子键.(2)Y的非金属性比N强(填“强”或“弱”),能证明此结论的事实是CO 2+H 2O+SiO32-=H 2SiO 3↓+CO 32-(用离子方程式表示).
(3)YX4的结构简式为CH4;分子里各原子的空间分布具有正四面体结构;在光照的条件下,将1mol YX4与1mol Cl2混合充分反应后,得到的产物最多有5种.
2.某有机物2.3g完全燃烧后,生成4.4g二氧化碳和2.7g水,则该有机物中( )
| A. | 只含有C、H两种元素 | |
| B. | 只含有C、O两种元素 | |
| C. | 含有C、H、O三种元素 | |
| D. | 一定含有C、H两种元素,不能确定是否含有O元素 |
1.短周期主族元素X、Y、Z、W原子序数依次增大.已知:X、Z同主族,X、Y、Z三种元素原子的最外层电子数之和为15,Y原子最外层电子数等于X原子最外层电子数的一半.下列叙述正确的是( )
| A. | 原子半径:X<W<Y<Z | |
| B. | X的氢化物稳定性大于Z的氢化物稳定性 | |
| C. | X在自然界中只能以化合态形式存在 | |
| D. | W的单质可使干燥的红色布条褪色 |
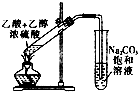
20.下列实验装置中正确的是( )
0 169706 169714 169720 169724 169730 169732 169736 169742 169744 169750 169756 169760 169762 169766 169772 169774 169780 169784 169786 169790 169792 169796 169798 169800 169801 169802 169804 169805 169806 169808 169810 169814 169816 169820 169822 169826 169832 169834 169840 169844 169846 169850 169856 169862 169864 169870 169874 169876 169882 169886 169892 169900 203614

| A. | 实验室用液溴、苯和铁制备溴苯时必须加热 | |
| B. | 实验室可用如图所示装置进行酯化实验 | |
| C. | 如果甲烷中混有少量乙烯,可以通过盛有酸性KMnO4溶液进行除杂 | |
| D. | 将加热后的铜丝多次插入乙醇中,乙醇中可以闻到刺激性气味 |