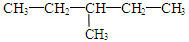9.下列实验现象与对应化学方程式都正确的是( )
| A. | 金属钠投入水中,浮在水面熔成小球,并在水面快速移动,得到的溶液显碱性;Na+H2O═NaOH+H2↑ | |
| B. | 氢气在氯气中安静的燃烧,发出淡蓝色火焰,瓶口出现白雾;H2+Cl2═2HCl | |
| C. | FeSO4溶液中加入NaOH溶液时,生成的白色絮状沉淀迅速变为灰绿色,最后变成红褐色; 2Fe(OH)2+O2+H2O═2 Fe(OH)3 | |
| D. | 向Na2SiO3溶液中逐滴加入稀盐酸,边加边振荡,有透明的硅酸凝胶产生;Na2SiO3+2HCl═H2SiO3(胶体)+2NaCl |
5.银质器皿日久表面会逐渐变黑,这是生成了Ag2S的缘故.根据电化学原理可进行如下处理:在铝质容器中加入食盐溶液,再将变黑的银器漫入该溶液中,一段时间后发现黑色会褪去.下列说法正确的是( )
| A. | 处理过程中银器一直保持恒重 | |
| B. | 食盐溶液作为电解质溶液形成原电池 | |
| C. | 银器为正极,Ag2S被还原生成单质银 | |
| D. | 黑色褪去的原因是黑色Ag2S转化为白色AgCl |
4.一定温度下,向一个容积为2L的真空密闭容器中(事先装入催化剂)通入1mol N2和3mol H2,发生下列反应:N2+3H2$?_{催化剂}^{高温、高压}$2NH3.3min后测得密闭容器内的压强是起始时的0.9倍,在此时间内v(H2)是( )
| A. | 0.2 mol/(L•min) | B. | 0.6 mol/(L•min) | C. | 0.1 mol/(L•min) | D. | 0.3 mol/(L•min) |
3.以下实验能获得成功的是( )
| A. | 将铁屑、溴水、苯混合制溴苯 | |
| B. | 在苯中滴入浓硝酸制硝基苯 | |
| C. | 用乙醇和乙酸混合共热制取乙酸乙酯 | |
| D. | 将铜丝在酒精灯加热后,立即伸入无水乙醇中,铜丝恢复成原来的红色 |
2.设nA为阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 0.1 mol•L-1NaCl溶液中含有0.1nA个Na+ | |
| B. | 标准状况下,22.4 L 苯含有nA个苯分子 | |
| C. | 7.8 g Na2O2与足量水反应转移0.2nA个电子 | |
| D. | 标准状况下,2.24 LCH4和C2H4混合气体中含有的H原子数为0.4nA |
1.某聚合物具有如下结构片段: ,其单体不可能具有的化学性质是( )
,其单体不可能具有的化学性质是( )
 ,其单体不可能具有的化学性质是( )
,其单体不可能具有的化学性质是( )| A. | 能使酸性KMnO4溶液褪色 | B. | 与NaOH溶液共热可生成一种钠盐 | ||
| C. | 能催化加氢生成2甲基丙酸甲酯 | D. | 能发生缩聚反应 |
20.研究人员研制利用低品位软锰矿浆(主要成分是MnO2)吸收硫酸厂的尾气SO2,制备硫酸锰的生产流程如图1:
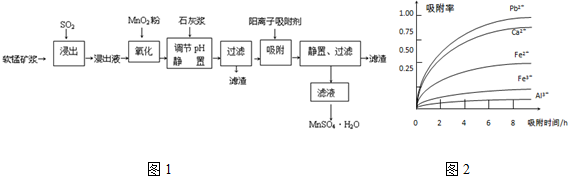
已知:浸出液的pH<2,其中的金属离子主要是Mn2+,还含有少量的Fe2+、Al3+、Ca2+、Pb2+等其他金属离子.PbO2的氧化性大于MnO2.有关金属离子的半径、形成氢氧化物沉淀时的pH见下表,阳离子吸附剂吸附金属离子的效果见图2.
(1)浸出过程中生成Mn2+反应的化学方程式为SO2+MnO2=MnSO4,
(2)Fe2+被氧化的过程中主要反应的离子方程式2Fe2++MnO2+4H+=2Fe3++Mn2++2H2O.
(3)在氧化后的液体中加入石灰浆,用于调节pH,pH应调节至4.7≤pH<8.3范围.
(4)阳离子吸附剂可用于除去杂质金属离子.请依据图、表信息回答,决定阳离子吸附剂吸附效果的因素有吸附时间、金属离子半径、金属离子电荷等(写二点).
(5)吸附步骤除去的主要离子为Pb2+、Ca2+.
(6)电解MnSO4、ZnSO4和H4SO4的混合溶液可制备MnO2和Zn,写出阳极的电极反应方程式Mn2+-2e-+2H2O=MnO2↓+4H+.
0 169686 169694 169700 169704 169710 169712 169716 169722 169724 169730 169736 169740 169742 169746 169752 169754 169760 169764 169766 169770 169772 169776 169778 169780 169781 169782 169784 169785 169786 169788 169790 169794 169796 169800 169802 169806 169812 169814 169820 169824 169826 169830 169836 169842 169844 169850 169854 169856 169862 169866 169872 169880 203614

已知:浸出液的pH<2,其中的金属离子主要是Mn2+,还含有少量的Fe2+、Al3+、Ca2+、Pb2+等其他金属离子.PbO2的氧化性大于MnO2.有关金属离子的半径、形成氢氧化物沉淀时的pH见下表,阳离子吸附剂吸附金属离子的效果见图2.
| 离子 | 离子半径(pm) | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe2+ | 74 | 7.6 | 9.7 |
| Fe3+ | 64 | 2.7 | 3.7 |
| Al3+ | 50 | 3.8 | 4.7 |
| Mn2+ | 80 | 8.3 | 9.8 |
| Pb2+ | 121 | 8.0 | 8.8 |
| Ca2+ | 99 | - | - |
(2)Fe2+被氧化的过程中主要反应的离子方程式2Fe2++MnO2+4H+=2Fe3++Mn2++2H2O.
(3)在氧化后的液体中加入石灰浆,用于调节pH,pH应调节至4.7≤pH<8.3范围.
(4)阳离子吸附剂可用于除去杂质金属离子.请依据图、表信息回答,决定阳离子吸附剂吸附效果的因素有吸附时间、金属离子半径、金属离子电荷等(写二点).
(5)吸附步骤除去的主要离子为Pb2+、Ca2+.
(6)电解MnSO4、ZnSO4和H4SO4的混合溶液可制备MnO2和Zn,写出阳极的电极反应方程式Mn2+-2e-+2H2O=MnO2↓+4H+.
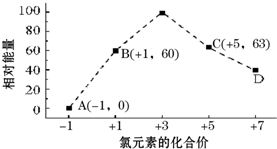 元素周期表中第ⅦA族元素的单质及其化合物的用途广泛.
元素周期表中第ⅦA族元素的单质及其化合物的用途广泛.
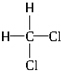 和
和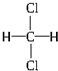 ③35Cl和37Cl
③35Cl和37Cl 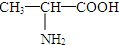 和 CH3-CH2-CH2-NO2 ⑤⑥(CH3)2CHCH(CH3)2和 (CH3)2CH(CH2)2CH3
和 CH3-CH2-CH2-NO2 ⑤⑥(CH3)2CHCH(CH3)2和 (CH3)2CH(CH2)2CH3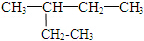 和
和