11.Bodensteins研究了下列反应:2HI(g)?H2(g)+I2(g)在716K时,气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如下表:
(1)716K时,可以表示可逆反应2HI(g)?H2(g)+I2(g)达到平衡的标志是AG.
A.碘化氢的生成速率和分解速率相等
B.单位时间内,1molH-H键生成,同时有2molH-I断开.
C.恒容的容器中,气体密度保持不变
D.恒容的容器中,压强保持不变
E.c(H2)和c(I2)的浓度相等
F.容器内气体的平均分子量保持不变
G.容器内气体颜色保持不变
(2)根据上述实验结果,该反应的平衡常数K的计算式为:$\frac{0.10{8}^{2}}{0.78{4}^{2}}$.(用表中具体数值代入,不计算结果)
(3)上述反应中,正反应速率为v正=k正x2(HI),逆反应速率为v逆=k逆x(H2)x(I2),其中
k正、k逆为速率常数,则k逆为$\frac{{k}_{正}}{K}$(以K和k正表示).若k正=0.0027min-1,在t=40min时,v正=1.95×10-3min-1.
0 169685 169693 169699 169703 169709 169711 169715 169721 169723 169729 169735 169739 169741 169745 169751 169753 169759 169763 169765 169769 169771 169775 169777 169779 169780 169781 169783 169784 169785 169787 169789 169793 169795 169799 169801 169805 169811 169813 169819 169823 169825 169829 169835 169841 169843 169849 169853 169855 169861 169865 169871 169879 203614
| t/min | 0 | 20 | 40 | 60 | 80 | 120 |
| X(HI) | 1 | 0.91 | 0.85 | 0.815 | 0.795 | 0.784 |
| X(HI) | 0 | 0.60 | 0.73 | 0.773 | 0.780 | 0.784 |
A.碘化氢的生成速率和分解速率相等
B.单位时间内,1molH-H键生成,同时有2molH-I断开.
C.恒容的容器中,气体密度保持不变
D.恒容的容器中,压强保持不变
E.c(H2)和c(I2)的浓度相等
F.容器内气体的平均分子量保持不变
G.容器内气体颜色保持不变
(2)根据上述实验结果,该反应的平衡常数K的计算式为:$\frac{0.10{8}^{2}}{0.78{4}^{2}}$.(用表中具体数值代入,不计算结果)
(3)上述反应中,正反应速率为v正=k正x2(HI),逆反应速率为v逆=k逆x(H2)x(I2),其中
k正、k逆为速率常数,则k逆为$\frac{{k}_{正}}{K}$(以K和k正表示).若k正=0.0027min-1,在t=40min时,v正=1.95×10-3min-1.
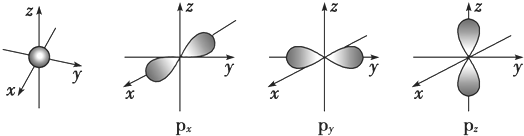
 .若元素X的原子最外层电子排布式为nsn-1npn+1,那么X的元素符号为S,原子的电子排布图为
.若元素X的原子最外层电子排布式为nsn-1npn+1,那么X的元素符号为S,原子的电子排布图为 .
.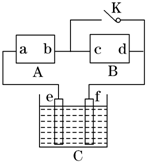 如图所示,A为直流电源,B为渗透饱和氯化钠溶液和酚酞试液的滤纸,C为电镀槽,接通电路后,发现B上的c点显红色,请填空:
如图所示,A为直流电源,B为渗透饱和氯化钠溶液和酚酞试液的滤纸,C为电镀槽,接通电路后,发现B上的c点显红色,请填空: