5.下列物质间的反应能用H++OH-═H2O表示的是( )
| A. | 醋酸和氢氧化钠 | B. | 盐酸和氨水 | ||
| C. | 硫酸和氢氧化钾 | D. | 碳酸氢钠和氢氧化钠 |
4.1mol H2表示的含义是( )
| A. | 1 mol 氢 | B. | 1 mol 氢气 | C. | 1 mol 氢分子 | D. | 1 mol 氢原子 |
3.下列名词不是物理量专有名词的是( )
| A. | 时间 | B. | 物质的量 | C. | 质量 | D. | 摩尔 |
19. (1)煤燃烧的反应热可通过以下两个途径来利用:a.利用煤在充足的空气中直接燃烧产生的反应热;b.先使煤与水蒸气反应得到氢气和一氧化碳,然后使得到的氢气和一氧化碳在充足的空气中燃烧.这两个过程的热化学方程式为:
(1)煤燃烧的反应热可通过以下两个途径来利用:a.利用煤在充足的空气中直接燃烧产生的反应热;b.先使煤与水蒸气反应得到氢气和一氧化碳,然后使得到的氢气和一氧化碳在充足的空气中燃烧.这两个过程的热化学方程式为:
a.C(s)+O2(g)═CO2(g)△H=E1①
b.C(s)+H2O(g)═CO(g)+H2(g)△H=E2②
H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=E3③
CO(g)+$\frac{1}{2}$O2(g)═CO2(g)△H=E4④
请表达E1、E2、E3、E4之间的关系为E2=E1-E3-E4.
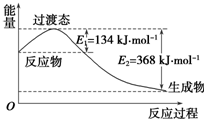
(2)如图所示是1摩尔NO2和1摩尔CO完全反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:NO2(g)+CO(g)═NO(g)+CO2(g)△H=-234 kJ•mol-1.
(3)化学反应的焓变与反应物和生成物的键能有关.已知某些化学键的键能如下表所示:
则反应:H2(g)+Cl2(g)═2HCl(g)的焓变△H=-185 kJ/mol.
 (1)煤燃烧的反应热可通过以下两个途径来利用:a.利用煤在充足的空气中直接燃烧产生的反应热;b.先使煤与水蒸气反应得到氢气和一氧化碳,然后使得到的氢气和一氧化碳在充足的空气中燃烧.这两个过程的热化学方程式为:
(1)煤燃烧的反应热可通过以下两个途径来利用:a.利用煤在充足的空气中直接燃烧产生的反应热;b.先使煤与水蒸气反应得到氢气和一氧化碳,然后使得到的氢气和一氧化碳在充足的空气中燃烧.这两个过程的热化学方程式为:a.C(s)+O2(g)═CO2(g)△H=E1①
b.C(s)+H2O(g)═CO(g)+H2(g)△H=E2②
H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=E3③
CO(g)+$\frac{1}{2}$O2(g)═CO2(g)△H=E4④
请表达E1、E2、E3、E4之间的关系为E2=E1-E3-E4.
(2)如图所示是1摩尔NO2和1摩尔CO完全反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:NO2(g)+CO(g)═NO(g)+CO2(g)△H=-234 kJ•mol-1.
(3)化学反应的焓变与反应物和生成物的键能有关.已知某些化学键的键能如下表所示:
| 共价键 | H-H | Cl-Cl | H-Cl |
| 键能/(kJ•mol-1) | 436 | 247 | 434 |
17.有4个系列同族元素的物质,101.3kPa时测定它们的沸点(℃)如下表所示:
对应表中内容,下列叙述中正确的是( )
0 169602 169610 169616 169620 169626 169628 169632 169638 169640 169646 169652 169656 169658 169662 169668 169670 169676 169680 169682 169686 169688 169692 169694 169696 169697 169698 169700 169701 169702 169704 169706 169710 169712 169716 169718 169722 169728 169730 169736 169740 169742 169746 169752 169758 169760 169766 169770 169772 169778 169782 169788 169796 203614
| ① | He-268.8 | (a)-249.5 | Ar-185.8 | Kr-151.7 |
| ② | F2-187.0 | Cl2-33.6 | (b) 58.7 | I2 184.0 |
| ③ | (c) 19.4 | HCl-84.0 | HBr-67.0 | HI-35.3 |
| ④ | H2O 100.0 | H2S-60.0 | (d)-42.0 | H2Te-1.8 |
| A. | 系列①的(a)物质中没有离子键,应有共价键和分子间作用力 | |
| B. | 系列③中(c)物质的沸点比HCl高是因为(c)中的共价键更牢固 | |
| C. | 系列②中(b)物质的元素的原子序数应为35,且该物质常温下为液态 | |
| D. | 系列④中H2O沸点变化出现反常,是因为分子内有氢键的影响 |
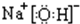

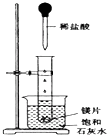 如图所示,把试管放入盛有25℃的饱和石灰水的烧杯中,试管中开始放入几小块镁片,再用滴管滴入5mL盐酸于试管中.试回答下列回答:
如图所示,把试管放入盛有25℃的饱和石灰水的烧杯中,试管中开始放入几小块镁片,再用滴管滴入5mL盐酸于试管中.试回答下列回答: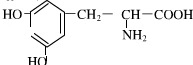 .
.