13.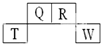 短周期元素Q、R、T、W在元素周期表中的位置如下,其中T原子的M层电子数比K层多2个,下列叙述不正确的是( )
短周期元素Q、R、T、W在元素周期表中的位置如下,其中T原子的M层电子数比K层多2个,下列叙述不正确的是( )
 短周期元素Q、R、T、W在元素周期表中的位置如下,其中T原子的M层电子数比K层多2个,下列叙述不正确的是( )
短周期元素Q、R、T、W在元素周期表中的位置如下,其中T原子的M层电子数比K层多2个,下列叙述不正确的是( )| A. | H2R2的分子中既含有极性共价键,又含有非极性共价键 | |
| B. | T的氧化物是一种良好的半导体材料 | |
| C. | Q、R的简单氢化物分子所含质子数、电子数与Ne分子相同 | |
| D. | Q的氢化物与W的氢化物反应有白烟现象,且生成物中既含有离子键,又含有共价键 |
12.糖类、脂肪和蛋白质是维持人体生命活动所必需的三大营养物质.以下叙述正确的( )
| A. | 植物油不能使溴水褪色 | B. | 淀粉水解的最终产物是葡萄糖 | ||
| C. | 葡萄糖、蔗糖都能水解 | D. | 油脂从分类上说属于不饱和烃 |
8.下列文字表述与对应的化学用语或名称关系正确的是( )
①131I与127I两核素互为同素异形体
②聚乙烯的结构简式为
③水晶的分子式为SiO2
④次氯酸分子的电子式为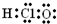
⑤新戊烷的系统命名为2,2-二甲基丙烷
⑥光气(COCl2)结构式为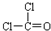
⑦苯分子的比例模型为
⑧NaH中阴离子的结构示意图
①131I与127I两核素互为同素异形体
②聚乙烯的结构简式为

③水晶的分子式为SiO2
④次氯酸分子的电子式为
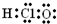
⑤新戊烷的系统命名为2,2-二甲基丙烷
⑥光气(COCl2)结构式为
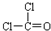
⑦苯分子的比例模型为

⑧NaH中阴离子的结构示意图

| A. | ①③④⑧ | B. | ②⑤⑥⑦ | C. | ②③⑤⑥⑦ | D. | ②④⑤⑥⑧ |
4.利用如图所示装置进行下列实验,能得出相应实验结论的是( )
0 169209 169217 169223 169227 169233 169235 169239 169245 169247 169253 169259 169263 169265 169269 169275 169277 169283 169287 169289 169293 169295 169299 169301 169303 169304 169305 169307 169308 169309 169311 169313 169317 169319 169323 169325 169329 169335 169337 169343 169347 169349 169353 169359 169365 169367 169373 169377 169379 169385 169389 169395 169403 203614
| 选项 | ① | ② | ③ | 实验结论 |  |
| A | 稀硫酸 | Na2S | AgNO3与AgCl的浊液 | Ksp(AgCl)>Ksp(Ag2S) | |
| B | 浓硫酸 | 蔗糖 | 溴水 | 浓硫酸具有脱水性、氧化性 | |
| C | 浓硫酸 | Na2SO3 | 品红溶液 | SO2具有漂白性 | |
| D | 浓硝酸 | Na2CO3 | Na2SiO3溶液 | 酸性:硝酸>碳酸>硅酸 |
| A. | A | B. | B | C. | C | D. | D |
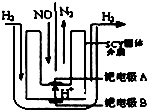 汽车尾气中NOx的消除及无害化处理引起社会广泛关注.
汽车尾气中NOx的消除及无害化处理引起社会广泛关注.
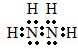
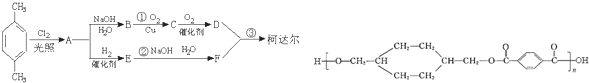
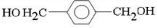 ;D
;D ;E
;E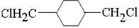
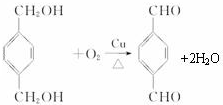 ,反应类型氧化反应
,反应类型氧化反应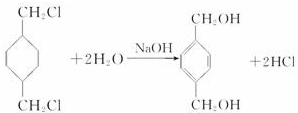 ,反应类型取代反应
,反应类型取代反应 $\stackrel{一定条件下}{→}$
$\stackrel{一定条件下}{→}$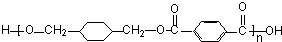 +(2n-1)H2O,反应类型缩聚反应.
+(2n-1)H2O,反应类型缩聚反应.