题目内容
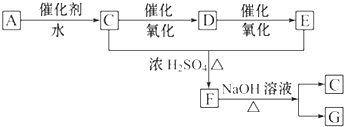
4.利用如图所示装置进行下列实验,能得出相应实验结论的是( )| 选项 | ① | ② | ③ | 实验结论 |  |
| A | 稀硫酸 | Na2S | AgNO3与AgCl的浊液 | Ksp(AgCl)>Ksp(Ag2S) | |
| B | 浓硫酸 | 蔗糖 | 溴水 | 浓硫酸具有脱水性、氧化性 | |
| C | 浓硫酸 | Na2SO3 | 品红溶液 | SO2具有漂白性 | |
| D | 浓硝酸 | Na2CO3 | Na2SiO3溶液 | 酸性:硝酸>碳酸>硅酸 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.稀硫酸与Na2S发生强酸制取弱酸的反应,生成H2S与③中硝酸银反应;
B.浓硫酸具有脱水性和氧化性,生成的二氧化硫与溴水发生氧化还原反应;
C.发生强酸制取弱酸的反应,生成二氧化硫可使品红褪色;
D.发生强酸制取弱酸的反应,但硝酸易挥发,硝酸与硅酸钠反应生成硅酸沉淀.
解答 解:A.稀硫酸与Na2S发生强酸制取弱酸的反应,生成H2S与③中硝酸银反应生成黑色沉淀,不发生沉淀的转化,则不能比较Ksp(AgCl)、Ksp(Ag2S),故A错误;
B.浓硫酸具有脱水性和氧化性,生成的二氧化硫与溴水发生氧化还原反应,溴水褪色,实验可完成,故B正确;
C.浓硫酸与亚硫酸钠反应生成二氧化硫,二氧化硫可使品红褪色,则SO2具有漂白性,故C正确;
D.发生强酸制取弱酸的反应,但硝酸易挥发,硝酸与硅酸钠反应生成硅酸沉淀,干扰碳酸、硅酸酸性比较,故D错误;
故选BC.
点评 本题考查化学实验方案的评价,为高频考点,涉及酸性比较、沉淀生成和转化、氧化还原反应及物质的性质等,把握物质性质及反应原理为解答的关键,侧重分析与实验能力的考查,题目难度不大.

练习册系列答案
相关题目
11.工业制ClO2的化学反应:2NaClO3+SO2+H2SO4=2ClO2+2NaHSO4,下列说法正确的是( )
| A. | NaClO3在反应中化合价降低,失去电子 | |
| B. | SO2在反应中发生氧化反应 | |
| C. | 2mol氧化剂在反应中得到2mol电子 | |
| D. | H2SO4在反应中作氧化剂 |
12.下列物质分类正确的是( )
| A. | FeO、Fe2O3、Na2O2均为碱性氧化物 | B. | 稀豆浆、硅酸、氯化铁溶液均为胶体 | ||
| C. | 烧碱、冰醋酸、四氯化碳均为电解质 | D. | 盐酸、水玻璃、氨水均为混合物 |
19.下列说法正确的是( )??
| A. | 苯不能使酸性KMnO4溶液褪色,与甲烷性质相似,因此苯为饱和烃 | |
| B. | 苯的结构简式为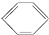 有三个双键,可与溴水发生加成反应 有三个双键,可与溴水发生加成反应 | |
| C. | 苯的6个碳原子和6个氢原子在同一平面内 | |
| D. | 将1 mL苯和1 mL水充分混合后静置,二者互溶 |
16.根据下列几种物质熔点和沸点的数据,判断下列说法中错误的是( )
注:AlCl3熔点在2.5×105Pa条件下测定.
| NaCl | MgCl2 | AlCl3 | SiCl4 | 单质B | |
| 熔点/℃ | 810 | 710 | 190 | -68 | 2 300 |
| 沸点/℃ | 1 465 | 1418 | 182.7 | 57 | 2 500 |
| A. | SiCl4是分子晶体 | B. | 单质B可能是原子晶体 | ||
| C. | AlCl3加热能升华 | D. | KCl的熔点大于810℃ |
13.下列各组内的物质不属于同系物的是( )
| A. | CH3-CH3 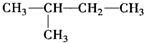 | |
| B. | CH2═CH-CH3 CH2═CH-CH2-CH3 | |
| C. | CH3-CH2-OH CH3-CH2-CH2-CH3 | |
| D. | 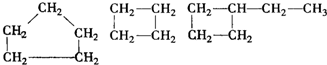 |
14.除去下列物质中的杂质(括号中的物质为杂质),请填写下列空白(注:加入的试剂请填写化学式):
| 物质 | 加入试剂 | 离子方程式 |
| NH4Cl(AlCl3)溶液 | NH3•H2O | Al3++3NH3•H2O=Al(OH)3↓+3NH4+ |
| NaHCO3(Na2CO3)溶液 | CO2 | CO32-+CO2+H2O=2HCO3- |
| Fe 粉(Al粉) | NaOH | 2Al+2OH-+2H2O=2AlO2-+3H2↑ |
| FeCl3(FeCl2)溶液 | Cl2 | 2Fe2++Cl2=2Fe3++2Cl- |