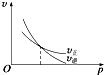
3. 已知某可逆反应mA(g)+nB(g)?qC(g)△H在密闭容器中进行.如图表示在不同时刻t、温度T和压强p下B物质在混合气体中的体积分数φ(B)的变化情况.下列推断中正确的是( )
已知某可逆反应mA(g)+nB(g)?qC(g)△H在密闭容器中进行.如图表示在不同时刻t、温度T和压强p下B物质在混合气体中的体积分数φ(B)的变化情况.下列推断中正确的是( )
 已知某可逆反应mA(g)+nB(g)?qC(g)△H在密闭容器中进行.如图表示在不同时刻t、温度T和压强p下B物质在混合气体中的体积分数φ(B)的变化情况.下列推断中正确的是( )
已知某可逆反应mA(g)+nB(g)?qC(g)△H在密闭容器中进行.如图表示在不同时刻t、温度T和压强p下B物质在混合气体中的体积分数φ(B)的变化情况.下列推断中正确的是( )| A. | p1>p2,T1<T2,m+n>q,△H<0 | B. | p1<p2,T1>T2,m+n>q,△H>0 | ||
| C. | p1>p2,T1<T2,m+n<q,△H<0 | D. | p1<p2,T1>T2,m+n<q,△H>0 |
2.(1)为进行Ⅰ项中的除杂实验(括号内为杂质),请从Ⅱ项中选出一种试剂,从Ⅲ项中选出一合适的实验操作方法分离,将标号填在后面的答案栏内.
(2)a.在洁净的试管中加入少量硝酸银溶液,再逐滴滴加稀氨水,现象是先生成白色沉淀,反应的离子方程式是①Ag++NH3•H2O=AgOH↓+NH4+;继续滴加至沉淀恰好溶解,即得银氨溶液,反应的离子方程式为②AgOH+2NH3=[Ag(NH3)2]++OH-;
b.向a中所得的银氨溶液中滴入少量葡萄糖溶液,混合均匀后,放在水浴中加热3min~5min,即可在试管内壁上形成银镜,则此反应的化学方程式为(葡萄糖的结构简式用G-CHO表示):③G-CHO+2Ag(NH3)2OH$\stackrel{△}{→}$G-COONH4+2Ag↓+3NH3+H2O.
0 169189 169197 169203 169207 169213 169215 169219 169225 169227 169233 169239 169243 169245 169249 169255 169257 169263 169267 169269 169273 169275 169279 169281 169283 169284 169285 169287 169288 169289 169291 169293 169297 169299 169303 169305 169309 169315 169317 169323 169327 169329 169333 169339 169345 169347 169353 169357 169359 169365 169369 169375 169383 203614
| Ⅰ除杂实验 | Ⅱ试剂 | Ⅲ操作方法 | 答案 | ||
| Ⅰ | Ⅱ | Ⅲ | |||
| ①苯(苯酚) | A.饱和Na2CO3溶液 B.NaCl晶体 C.NaOH溶液 D.CaO | a.蒸馏 b.分液 c.盐析、过滤 d.萃取 | ① | ||
| ②乙醇(水) | ② | ||||
| ③肥皂(甘油、水) | ③ | ||||
| ④乙酸乙酯(乙酸) | ④ | ||||
b.向a中所得的银氨溶液中滴入少量葡萄糖溶液,混合均匀后,放在水浴中加热3min~5min,即可在试管内壁上形成银镜,则此反应的化学方程式为(葡萄糖的结构简式用G-CHO表示):③G-CHO+2Ag(NH3)2OH$\stackrel{△}{→}$G-COONH4+2Ag↓+3NH3+H2O.
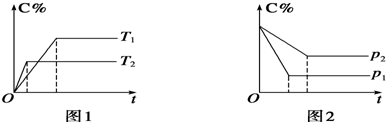


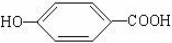
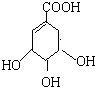 莽草酸是合成治疗禽流感的药物--达菲(Tamiflu)的原料之一.莽草酸是A的一种异构体.A的结构简式如图:
莽草酸是合成治疗禽流感的药物--达菲(Tamiflu)的原料之一.莽草酸是A的一种异构体.A的结构简式如图: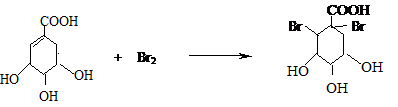 .
.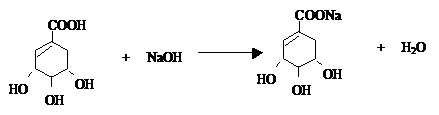 .
. ),其反应类型消去反应.
),其反应类型消去反应.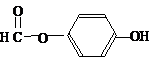 或
或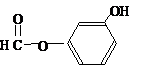 或
或 .
.