9.工业上由氯气与消石灰反应制备漂粉精,其化学式可以用xCa(ClO)2•yCaCl2•zCa(OH)2(x、y、z为简单整数)来表示.某兴趣小组同学对漂粉精进行定性、定量探究如下:
Ⅰ.证明漂粉精中含有CaCl2
①向漂粉精固体中滴加足量浓硫酸,观察到黄绿色气体生成.写出生成黄绿色气体的化学反应方程式:Ca(ClO)2+CaCl2+4H2SO4(浓)=2Ca(HSO4)2+2Cl2↑+2H2O
(或Ca(ClO)2+CaCl2+2H2SO4(浓)=CaSO4+2Cl2↑+2H2O).
②将生成的黄绿色气体缓缓通过足量碱石灰,碱石灰增重,并收集到无色气体.推测生成气体中除Cl2,还含有HCl、O2(填化学式).
Ⅱ.证明漂粉精中含有Ca(OH)2[已知电离常数:Ka1(H2CO3)>Ka(HClO)>Ka2(H2CO3)]
①将少量漂粉精溶于水后,测定其pH值为12.3.采用的测定方法可能是c(选填答案编号).
a.使用广泛pH试纸 b.使用精密pH试纸c.使用pH计 d.以酚酞为指示剂进行酸碱中和滴定
②下列探究步骤的设计中,对证明该结论无意义的是a(选填答案编号).
a.向漂粉精溶液中通入适量CO2,测定溶液的pH值变化
b.向漂粉精溶液中加入适量碳酸氢钠固体,测定溶液pH值变化
c.向漂粉精溶液中加入适量亚硫酸钠固体,测定溶液pH值变化 ③
Ⅲ.测定漂粉精中有效成分的含量
【实验原理】ClO-+2I-+2H+=Cl-+I2+H2O; I2+2S2O32-=2I-+S4O62-
【实验步骤】
i.称取7.740g漂粉精固体,溶解,配成250mL溶液;
ii.量取该溶液5.00mL于锥形瓶,加入过量KI溶液、酸化,并加入指示剂;
iii.用0.100mol/L Na2S2O3标准溶液滴定至终点,记录始末读数;
iv.重复ii、iii操作,记录始末读数.
①该实验中要使用的定量仪器除电子天平外还有滴定管、250mL容量瓶(写名称).
②步骤ii中加入的指示剂为淀粉(写名称),当观察到溶液由蓝色变为无色,且半分钟内不变化
时,达到滴定终点.
③实验数据如下:
若理论上滴定时消耗标准溶液27.00mL,则相对误差为-0.185%(保留3位有效数字).
④该漂粉精中Ca(ClO)2的质量分数为(以理论值计)0.624(保留3位有效数字).
Ⅰ.证明漂粉精中含有CaCl2
①向漂粉精固体中滴加足量浓硫酸,观察到黄绿色气体生成.写出生成黄绿色气体的化学反应方程式:Ca(ClO)2+CaCl2+4H2SO4(浓)=2Ca(HSO4)2+2Cl2↑+2H2O
(或Ca(ClO)2+CaCl2+2H2SO4(浓)=CaSO4+2Cl2↑+2H2O).
②将生成的黄绿色气体缓缓通过足量碱石灰,碱石灰增重,并收集到无色气体.推测生成气体中除Cl2,还含有HCl、O2(填化学式).
Ⅱ.证明漂粉精中含有Ca(OH)2[已知电离常数:Ka1(H2CO3)>Ka(HClO)>Ka2(H2CO3)]
①将少量漂粉精溶于水后,测定其pH值为12.3.采用的测定方法可能是c(选填答案编号).
a.使用广泛pH试纸 b.使用精密pH试纸c.使用pH计 d.以酚酞为指示剂进行酸碱中和滴定
②下列探究步骤的设计中,对证明该结论无意义的是a(选填答案编号).
a.向漂粉精溶液中通入适量CO2,测定溶液的pH值变化
b.向漂粉精溶液中加入适量碳酸氢钠固体,测定溶液pH值变化
c.向漂粉精溶液中加入适量亚硫酸钠固体,测定溶液pH值变化 ③
Ⅲ.测定漂粉精中有效成分的含量
【实验原理】ClO-+2I-+2H+=Cl-+I2+H2O; I2+2S2O32-=2I-+S4O62-
【实验步骤】
i.称取7.740g漂粉精固体,溶解,配成250mL溶液;
ii.量取该溶液5.00mL于锥形瓶,加入过量KI溶液、酸化,并加入指示剂;
iii.用0.100mol/L Na2S2O3标准溶液滴定至终点,记录始末读数;
iv.重复ii、iii操作,记录始末读数.
①该实验中要使用的定量仪器除电子天平外还有滴定管、250mL容量瓶(写名称).
②步骤ii中加入的指示剂为淀粉(写名称),当观察到溶液由蓝色变为无色,且半分钟内不变化
时,达到滴定终点.
③实验数据如下:
| 实验编号 | 1 | 2 | 3 |
| 消耗Na2S2O3体积/mL | 26.90 | 27.00 | 26.95 |
④该漂粉精中Ca(ClO)2的质量分数为(以理论值计)0.624(保留3位有效数字).
7.在烷烃分子中的基团:-CH3,-CH2-, ,
, 中的碳原子分别称为伯,仲,叔,季碳原子,数目分别用n1,n2,n3,n4来表示.若烷烃分子中氢原子数n0,则不同烷烃分子中各原子数的关系不正确的是( )
中的碳原子分别称为伯,仲,叔,季碳原子,数目分别用n1,n2,n3,n4来表示.若烷烃分子中氢原子数n0,则不同烷烃分子中各原子数的关系不正确的是( )
 ,
, 中的碳原子分别称为伯,仲,叔,季碳原子,数目分别用n1,n2,n3,n4来表示.若烷烃分子中氢原子数n0,则不同烷烃分子中各原子数的关系不正确的是( )
中的碳原子分别称为伯,仲,叔,季碳原子,数目分别用n1,n2,n3,n4来表示.若烷烃分子中氢原子数n0,则不同烷烃分子中各原子数的关系不正确的是( )| A. | n0=3n1+2n2+n3 | B. | n0=2(n1+n2+n3+n4)+2 | ||
| C. | n1=n3+2n4+2 | D. | n1=n3+2n2+2 |
6.含有碳氢氧三种元素,相对分子质量为60的有机物,当其与钠反应放出氢气时,其结构有( )
| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
5.下列实验方法不正确的是( )
| A. | 用重结晶法可除去KNO3晶体中混有少量NaCl晶体 | |
| B. | 实验室制取乙酸丁酯时用水浴加热 | |
| C. | 在硫酸钡悬浊液中加入足量饱和碳酸钠溶液可将其转化为碳酸钡 | |
| D. | 二氧化硫分别通入到硫化钠和硝酸钡溶液中产生沉淀可证明二氧化硫的氧化性和还原性 |
4.已知短周期元素的离子aAm+、bBn+、cCm-、dDn-(m>n)都具有相同的电子层结构,则下列叙述正确的是( )
| A. | 原子半径:A>B>C>D | |
| B. | 离子的还原性:cCm-比dDn-弱 | |
| C. | 离子半径:C>D>B>A | |
| D. | 气态氢化物的稳定性HmC一定大于HnD |
3.下列各组化合物的性质比较,不正确的是( )
| A. | 非金属性:F>O>S | B. | 稳定性:PH3>H2S>HCl | ||
| C. | 碱性:NaOH>Mg(OH)2>Al(OH)3 | D. | 酸性:HClO4>HBrO4>HIO4 |
2.下列各组物质中,其互称为同分异构体的是( )
| A. | 12C、13C和14C | B. | O2和O3 | ||
| C. | CH3CH2CH2CH3和CH3CH (CH3)CH3 | D. | CH3CH2CH3和CH3CH2CH2CH3 |
1.元素R的气态氢化物化学式为H2R,下列叙述不正确的是( )
0 169068 169076 169082 169086 169092 169094 169098 169104 169106 169112 169118 169122 169124 169128 169134 169136 169142 169146 169148 169152 169154 169158 169160 169162 169163 169164 169166 169167 169168 169170 169172 169176 169178 169182 169184 169188 169194 169196 169202 169206 169208 169212 169218 169224 169226 169232 169236 169238 169244 169248 169254 169262 203614
| A. | 该元素的原子最外层上有6个电子 | |
| B. | 该元素最高价氧化物的化学式为RO2 | |
| C. | 该元素是非金属元素 | |
| D. | 该元素最高价含氧酸的化学式为H2RO4 |
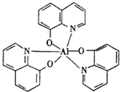 2012年10月1日起,我国将逐步淘汰白炽灯而采用高效照明的电致发光产品,电致发光材料有掺杂Mn2+和Cu2+的硫化锌、蒽单晶、8-羟基喹啉铝等.
2012年10月1日起,我国将逐步淘汰白炽灯而采用高效照明的电致发光产品,电致发光材料有掺杂Mn2+和Cu2+的硫化锌、蒽单晶、8-羟基喹啉铝等.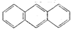 属于非极性(填“极性”“非极性”)分子
属于非极性(填“极性”“非极性”)分子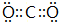 ,Y可形成分子晶体.过量的Y与氢氧化钠反应后的丁溶液与甲和氢氧化钠反应后的戊溶液发生的离子反应为HCO3-+AlO2-+H2O=Al(OH)3↓+CO32-.
,Y可形成分子晶体.过量的Y与氢氧化钠反应后的丁溶液与甲和氢氧化钠反应后的戊溶液发生的离子反应为HCO3-+AlO2-+H2O=Al(OH)3↓+CO32-.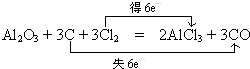 .
.