题目内容
3.下列各组化合物的性质比较,不正确的是( )| A. | 非金属性:F>O>S | B. | 稳定性:PH3>H2S>HCl | ||
| C. | 碱性:NaOH>Mg(OH)2>Al(OH)3 | D. | 酸性:HClO4>HBrO4>HIO4 |
分析 A.同周期元素从左到右元素的非金属性逐渐增强,同主族从上到下非金属性减弱;
B.元素的非金属性越强,对应的氢化物越稳定;
C.元素的金属性越强,对应的最高价氧化物的水化物的碱性越强;
D.元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强.
解答 解:A.同周期元素从左到右元素的非金属性逐渐增强,则非金属性:F>O,同主族元素从上到下元素的非金属性逐渐减弱,则非金属性:O>S,则有非金属性:F>O>S,故A正确;
B.非金属性:Cl>S>P,元素的非金属性越强,对应的氢化物越稳定,则稳定性:PH3<H2S<HCl,故B错误;
C.金属性:Na>Mg>Al,元素的金属性越强,对应的最高价氧化物的水化物的碱性越强,则碱性:NaOH>Mg(OH)2>Al(OH)3,故C正确;
D.非金属性:Cl>Br>I,元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强,则酸性:HClO4>HBrO4>HIO4,故D正确,故选B.
点评 本题考查元素的非金属性、金属性的比较,题目难度不大,注意元素的性质与对应单质、化合物性质之间的关系.

练习册系列答案
 赢在课堂名师课时计划系列答案
赢在课堂名师课时计划系列答案 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案
相关题目
13.有机物的结构简式如图: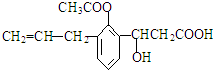 ,则此有机物可发生的反应类型有:( )①取代 ②加成 ③酯化 ④水解 ⑤氧化 ⑥中和.
,则此有机物可发生的反应类型有:( )①取代 ②加成 ③酯化 ④水解 ⑤氧化 ⑥中和.
 ,则此有机物可发生的反应类型有:( )①取代 ②加成 ③酯化 ④水解 ⑤氧化 ⑥中和.
,则此有机物可发生的反应类型有:( )①取代 ②加成 ③酯化 ④水解 ⑤氧化 ⑥中和.| A. | ①②④⑤⑥ | B. | ②③④⑤ | C. | ①②③④⑤⑥ | D. | ②③④⑤⑥ |
14.下列有关物质的性质,说法正确的是( )
| A. | SiO2既能与氢氟酸反应,又能与烧碱反应,所以它是两性氧化物 | |
| B. | Cl2、SO2都能使紫色石蕊试液与品红溶液褪色 | |
| C. | 相同质量的Cu分别与过量的体积相同的浓硝酸、稀硝酸反应,反应中铜失去的电子数相等 | |
| D. | 32g Cu与50mL 18.4mol/L的硫酸溶液共热,充分反应后,被还原的H2SO4为0.46mol |
11.有机物A的结构如右图所示,下列有关判断,正确的是( )


| A. | 1mol该有机物最多能与含2mol Br2的水溶液反应 | |
| B. | A的核磁共振氢谱图上有7个吸收峰 | |
| C. | A能发生银镜反应和酯化反应 | |
| D. | 与足量NaOH溶液反应转变成 |
18.SK-Ⅱ是护肤品当中的著名品牌,但是最近在全国各地发现SK-Ⅱ护肤品当中铬或者钕等重金属含量超标,人们纷纷引起退货洪朝.下面有关铬或者钕的描述中,正确的是( )
| A. | 将含有铬离子或者钕离子的盐溶液加入蛋白质溶液后,蛋白质仍然可以通过滤纸 | |
| B. | 24Cr的一种原子的质量数为48,该原子24Cr3+核外有24个电子 | |
| C. | 酒精测定仪中发生的化学反应如下:3CH3CH2OH+2K2Cr2O7+8H2SO4═3CH3COOH+2Cr2(SO4)3+2K2SO4+11H2O,其中K2Cr2O7起到是氧化剂的作用 | |
| D. | CrO42-和Cr2O72-中Cr元素的化合价相同 |
12.“喷水溶液法”是日本科学家最近研制的一种使沙漠变绿洲的技术,先是在沙漠中喷洒一定量的聚丙烯酸酯水溶液,水溶液中的高分子与沙粒结合,在地表下30-50cm处形成一个厚0.5cm的隔水层,既能阻止地下的盐分上升,又有蓄积雨水的作用,下列对聚丙烯酸酯的说法中正确的是( )
| A. | 聚丙烯酸酯的单体的结构简式为:CH2=CH-COOR | |
| B. | 聚丙烯酸酯在一定条件下能发生加成反应 | |
| C. | 聚丙烯酸酯不能发生水解反应 | |
| D. | 聚丙烯酸酯有固定的熔沸点 |
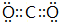 ,Y可形成分子晶体.过量的Y与氢氧化钠反应后的丁溶液与甲和氢氧化钠反应后的戊溶液发生的离子反应为HCO3-+AlO2-+H2O=Al(OH)3↓+CO32-.
,Y可形成分子晶体.过量的Y与氢氧化钠反应后的丁溶液与甲和氢氧化钠反应后的戊溶液发生的离子反应为HCO3-+AlO2-+H2O=Al(OH)3↓+CO32-.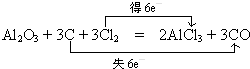 .
.
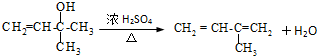 .
.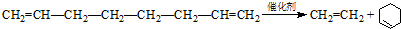 .
. 外,还有
外,还有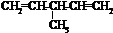 、
、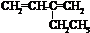 (填结构简式,已知
(填结构简式,已知 不稳定).
不稳定).