4.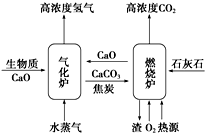 Ⅰ、由生物质能通过绿色化学途径制取氢气是当前能源发展的一个重要方向.如图表示的是以CaO为吸收体,将生物质经与水蒸气反应制取H2的流程(生物质简写为C).
Ⅰ、由生物质能通过绿色化学途径制取氢气是当前能源发展的一个重要方向.如图表示的是以CaO为吸收体,将生物质经与水蒸气反应制取H2的流程(生物质简写为C).
其中气化炉和燃烧炉中分别发生的主要反应如表所示:
请回答下列问题:
(1)气化炉中的总反应为C(s)+2H2O(g)+CaO(s)═CaCO3(s)+2H2(g)△H=-87.9 kJ•mol-1.
(2)燃烧炉中反应⑤所需的能量由反应④提供.如果生成1mol CaO,至少需通入纯氧0.453mol.(留三位小数点)
(3)下表列出的是当只改变温度或压强时,反应⑤中CO2的浓度和CaCO3的残留率的变化.
由表中数据可知,随着温度升高,反应⑤K值增大(填“增大”、“减小”或“不变”),T1>T2(填“>”或“<”,下同);随着压强增大,CaCO3的分解率减小,则p1>p2.
Ⅱ、以熔融碳酸盐(Li2CO3)为电解质,一氧化碳-空气燃料电池的负极反应式为CO-2e-+CO32-=2CO2.在标准状况下,11.2L氧气参与反应,理论上转移的电子数为2NA(或1.204×1024).
 Ⅰ、由生物质能通过绿色化学途径制取氢气是当前能源发展的一个重要方向.如图表示的是以CaO为吸收体,将生物质经与水蒸气反应制取H2的流程(生物质简写为C).
Ⅰ、由生物质能通过绿色化学途径制取氢气是当前能源发展的一个重要方向.如图表示的是以CaO为吸收体,将生物质经与水蒸气反应制取H2的流程(生物质简写为C).其中气化炉和燃烧炉中分别发生的主要反应如表所示:
| 气化炉 | 燃烧炉 |
| ①C(s)+H2O(g)?CO(g)+H2(g)△H=+131.6kJ•mol-1 ②CO(g)+H2O(g)?CO2(g)+H2(g)△H=-41.2kJ•mol-1 ③CaO(s)+CO2(g)?CaCO3(s)△H=-178.3kJ•mol-1 | ④C(s)+O2(g)═CO2(g) △H=-393.8kJ•mol-1 ⑤CaCO3(s)?CaO(s)+CO2(g) K |
(1)气化炉中的总反应为C(s)+2H2O(g)+CaO(s)═CaCO3(s)+2H2(g)△H=-87.9 kJ•mol-1.
(2)燃烧炉中反应⑤所需的能量由反应④提供.如果生成1mol CaO,至少需通入纯氧0.453mol.(留三位小数点)
(3)下表列出的是当只改变温度或压强时,反应⑤中CO2的浓度和CaCO3的残留率的变化.
 | 0 | 5 | 10 | 15 | 20 | 25 |
| T1 | 0 | 1.5 | 2.3 | 4.0 | 4.0 | 4.0 |
| T2 | 0 | 1.0 | 1.8 | 2.8 | 3.1 | 3.1 |
 | 0 | 5 | 10 | 15 | 20 | 25 |
| p1 | 1 | 0.90 | 0.83 | 0.75 | 0.75 | 0.75 |
| p2 | 1 | 0.58 | 0.35 | 0.31 | 0.30 | 0.30 |
Ⅱ、以熔融碳酸盐(Li2CO3)为电解质,一氧化碳-空气燃料电池的负极反应式为CO-2e-+CO32-=2CO2.在标准状况下,11.2L氧气参与反应,理论上转移的电子数为2NA(或1.204×1024).
2.下列说法中正确的是( )
| A. | NaOH溶液于水时仅破坏了离子键而未破坏共价键 | |
| B. | NH4Cl溶解于水时不仅破坏了离子键还破坏了共价键 | |
| C. | H2SO4溶解于水时,所有的共价键都被破坏 | |
| D. | HCl溶解于水时电离出H+和Cl-,所以共价键变成了离子键 |
1.下表中对应关系正确的是( )
| A | CH3CH3+Cl2$\stackrel{光照}{→}$CH3CH2Cl+HCl CH2=CH2+HCl→CH3CH2Cl | 均为取代反应 |
| B | 由油脂得到甘油 由淀粉得到葡萄糖 | 均发生了水解反应 |
| C | 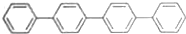 的一氯代物 的一氯代物 | 有5种 |
| D | 蛋白质水解的最终产物 | 多肽 |
| A. | A | B. | B | C. | C | D. | D |
20.将a g二氧化锰粉末加入cL b mol•L-1的浓盐酸中加热完全溶解,反应中转移电子d个,设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 可以收集到氯气$\frac{22.4b}{2{N}_{A}}$L | B. | 反应后Cl-数目为bc-d | ||
| C. | NA可表示为$\frac{87d}{2a}$ | D. | 反应后溶液中的H+数目为bc-2d |
19.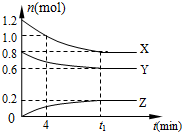 在2L密闭容器中有X、Y、Z三种气体间恒温下发生的可逆反应,它们的物质的量随时间变化而变化的曲线如图所示.下列分析正确的是( )
在2L密闭容器中有X、Y、Z三种气体间恒温下发生的可逆反应,它们的物质的量随时间变化而变化的曲线如图所示.下列分析正确的是( )
 在2L密闭容器中有X、Y、Z三种气体间恒温下发生的可逆反应,它们的物质的量随时间变化而变化的曲线如图所示.下列分析正确的是( )
在2L密闭容器中有X、Y、Z三种气体间恒温下发生的可逆反应,它们的物质的量随时间变化而变化的曲线如图所示.下列分析正确的是( )| A. | 4 min内 v(Z)=0.025 mol•L-1•min-1 | |
| B. | Y的平衡转化率为75% | |
| C. | 平衡常数K=(25/12)(mol•L-1)-2 | |
| D. | t1 min时充入少量He,平衡向正向移动 |
18.除去试管中银镜的实验方案如下表所列,实验操作中均经振荡、充分反应:
下列分析结论正确的是( )
| 方案 | 实验操作 | 现象 |
| Ⅰ | 将2mL 2mol/L Fe(NO3)3溶液加入有银镜的试管中 | 银镜较迅速消失 试管口产生红棕色气体 |
| Ⅱ | 将2mL2mol/L Fe2(SO4)3溶液加入有银镜的试管中 | 银镜减少但未消失 |
| Ⅲ | 将2mL 2mol/L FeCl3溶液加入有银镜的试管中 | 银镜较迅速消失 有白色沉淀生成 |
| A. | 方案Ⅰ说明Fe3+ 氧化了Ag | |
| B. | 方案Ⅱ涉及反应之一为Fe3++Ag?Fe2++Ag+ | |
| C. | 方案Ⅱ、Ⅲ对比说明SO42-比Cl-更易沉淀Ag+ | |
| D. | 三个方案对比说明方案Ⅰ是除去银镜的最佳方案 |
17. X、Y、Z、W四种短周期元素(其中只有一种是金属元素)在周期表中的相对位置如图所示.下列说法正确的是( )
X、Y、Z、W四种短周期元素(其中只有一种是金属元素)在周期表中的相对位置如图所示.下列说法正确的是( )
 X、Y、Z、W四种短周期元素(其中只有一种是金属元素)在周期表中的相对位置如图所示.下列说法正确的是( )
X、Y、Z、W四种短周期元素(其中只有一种是金属元素)在周期表中的相对位置如图所示.下列说法正确的是( )| A. | 简单离子的半径:X3+>Z3- | |
| B. | 元素Z的最外层电子可能为6 | |
| C. | 元素Y的最高价氧化物的水化物可能是强酸 | |
| D. | 元素W的最高价氧化物的水化物属于共价化合物 |
16.下列说法不正确的是( )
0 168571 168579 168585 168589 168595 168597 168601 168607 168609 168615 168621 168625 168627 168631 168637 168639 168645 168649 168651 168655 168657 168661 168663 168665 168666 168667 168669 168670 168671 168673 168675 168679 168681 168685 168687 168691 168697 168699 168705 168709 168711 168715 168721 168727 168729 168735 168739 168741 168747 168751 168757 168765 203614
| A. | 含氟氯代烃的废弃发泡塑料对臭氧层无影响 | |
| B. | 煤的气化是高效且清洁地利用煤炭的重要途径 | |
| C. | 将聚乙烯塑料经热裂解可得重新利用的小分子 | |
| D. | 使用无磷洗衣粉可缓解水体富营养化的趋势 |