题目内容
2.下列说法中正确的是( )| A. | NaOH溶液于水时仅破坏了离子键而未破坏共价键 | |
| B. | NH4Cl溶解于水时不仅破坏了离子键还破坏了共价键 | |
| C. | H2SO4溶解于水时,所有的共价键都被破坏 | |
| D. | HCl溶解于水时电离出H+和Cl-,所以共价键变成了离子键 |
分析 A.NaOH溶于水时,NaOH在水分子作用下发生电离;
B、NH4Cl溶解于水发生电离,离子键被破坏;
C、硫酸溶解于水发生电离,共价键被破坏;
D、HCl属于共价化合物,只存在共价键.
解答 解:A.NaOH溶于水时,NaOH在水分子作用下发生电离,所以破坏了离子键而未破坏共价键,故A正确;
B、NH4Cl溶解于水发生电离,离子键被破坏,无共价键破坏,故B错误;
C、硫酸溶解于水发生电离,共价键被破坏,而硫与氧之间的共价键未被破坏,故C错误;
D、HCl属于共价化合物,只存在共价键,所以无离子键,故D错误;
故选A.
点评 本题考查化学键,明确物质的构成微粒及化学变化的实质是解本题关键,采用举例法分析解答即可,题目难度中等.

练习册系列答案
 金钥匙试卷系列答案
金钥匙试卷系列答案
相关题目
15.氰气(CN)2性质与卤素相似,分子中4个原子处于同一直线.下列叙述正确的是( )
| A. | 分子中只存在极性键 | B. | 在氰气中N、C的化合价为0 | ||
| C. | CN的电子式: | D. | 能与烯烃发生加成反应 |
13.对羟基扁桃酸是药物合成的重要中间体,它可由苯酚和乙醛酸反应制得.下列有关说法正确的是( )


| A. | 对羟基扁桃酸可以发生消去反应、取代反应和缩聚反应 | |
| B. | 苯酚和对羟基扁桃酸是同系物 | |
| C. | 乙醛酸与H2在热的镍催化下反应生成乙二醇 | |
| D. | 在核磁共振氢谱中对羟基扁桃酸应该有6个吸收峰 |
10.下列装置能达到对应实验目的是( )
| A. |  分离碘与沙子 | B. | 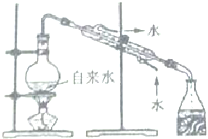 实验室制取蒸馏水 | ||
| C. | 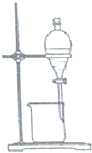 乙醇提取碘水中的碘 | D. | 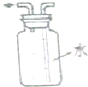 收集氨气 |
17. X、Y、Z、W四种短周期元素(其中只有一种是金属元素)在周期表中的相对位置如图所示.下列说法正确的是( )
X、Y、Z、W四种短周期元素(其中只有一种是金属元素)在周期表中的相对位置如图所示.下列说法正确的是( )
 X、Y、Z、W四种短周期元素(其中只有一种是金属元素)在周期表中的相对位置如图所示.下列说法正确的是( )
X、Y、Z、W四种短周期元素(其中只有一种是金属元素)在周期表中的相对位置如图所示.下列说法正确的是( )| A. | 简单离子的半径:X3+>Z3- | |
| B. | 元素Z的最外层电子可能为6 | |
| C. | 元素Y的最高价氧化物的水化物可能是强酸 | |
| D. | 元素W的最高价氧化物的水化物属于共价化合物 |
14.只用一种试剂就能将甲苯、己烯、四氯化碳和碘化钾溶液区分开,该试剂可以是( )
| A. | 酸性高锰酸钾溶液 | B. | 溴化钠溶液 | ||
| C. | 溴水 | D. | 硝酸银溶液 |
11.X、Y、Z、W均为短周期元素,它们在元素周期表中相对位置如图所示.Z为地壳中含量最多的金属元素,下列说法中正确的是( )
| X | Y | |||
| Z | W | Q |
| A. | X、Y、W三种元素最低价氢化物的沸点依次升高 | |
| B. | 原子半径:Q>W>Z>Y>X | |
| C. | 最高价氧化物对应水化物的酸性:Q>W>Z | |
| D. | X及Q的气态氢化物相反应,形成的化合物为离子化合物 |
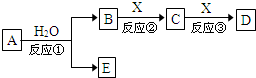 由短周期元素组成的中学常见物质A、B、C、D、E存在图转化关系(部分生成物和反应条件略).
由短周期元素组成的中学常见物质A、B、C、D、E存在图转化关系(部分生成物和反应条件略).