19. 将一根较纯铁棒垂直没入水中,由于深水处溶氧量较少,一段时间后发现AB段产生较多铁锈,BC段腐蚀严重,下列关于此现象的说法错误的是( )
将一根较纯铁棒垂直没入水中,由于深水处溶氧量较少,一段时间后发现AB段产生较多铁锈,BC段腐蚀严重,下列关于此现象的说法错误的是( )
 将一根较纯铁棒垂直没入水中,由于深水处溶氧量较少,一段时间后发现AB段产生较多铁锈,BC段腐蚀严重,下列关于此现象的说法错误的是( )
将一根较纯铁棒垂直没入水中,由于深水处溶氧量较少,一段时间后发现AB段产生较多铁锈,BC段腐蚀严重,下列关于此现象的说法错误的是( )| A. | 铁棒AB段发生反应为O2+4e-+2H2O=4OH- | |
| B. | 腐蚀过程中在铁棒上会产生微电流,且方向是AB段到BC段 | |
| C. | 向水中加入一定量硫酸钾固体后,对铁棒的生锈速率几乎无影响 | |
| D. | 产生这种现象的本质原因是铁棒所处的化学环境不同 |
18.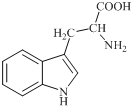 色氨酸是植物体内生长素生物合成重要的前体物质,普遍存在于高等植物中.纯净的色氨酸为白色或微黄色结晶,微溶于水易溶于盐酸或氢氧化钠,其结构如图所示,下列关于色氨酸的说法不正确的是( )
色氨酸是植物体内生长素生物合成重要的前体物质,普遍存在于高等植物中.纯净的色氨酸为白色或微黄色结晶,微溶于水易溶于盐酸或氢氧化钠,其结构如图所示,下列关于色氨酸的说法不正确的是( )
 色氨酸是植物体内生长素生物合成重要的前体物质,普遍存在于高等植物中.纯净的色氨酸为白色或微黄色结晶,微溶于水易溶于盐酸或氢氧化钠,其结构如图所示,下列关于色氨酸的说法不正确的是( )
色氨酸是植物体内生长素生物合成重要的前体物质,普遍存在于高等植物中.纯净的色氨酸为白色或微黄色结晶,微溶于水易溶于盐酸或氢氧化钠,其结构如图所示,下列关于色氨酸的说法不正确的是( )| A. | 色氨酸的分子式为C11H12N2O2 | |
| B. | 色氨酸能发生取代、加成、酯化、中和反应 | |
| C. | 色氨酸微溶于水而易溶于酸或碱溶液是因为其与酸、碱都能反应生成盐 | |
| D. | 将色氨酸与甘氨酸(NH2CH2COOH)混合,在一定条件下最多可形成三种二肽 |
17.X、Y、Z、W为四种短周期元素.已知X、Y的原子得到两个电子形成稀有气体原子结构时,X放出的能量大于Y.Z、W的原子失去一个电子形成稀有气体原子结构时,W吸收的能量大于Z.则下列关于四种元素的说法正确的是( )
| A. | W、X两元素对应的单质发生反应只能得到W2X | |
| B. | 由X、Y、Z三种元素组成的物质其水溶液一定呈中性 | |
| C. | 1 mol Z2X2与足量水反应可得气体11.2 L | |
| D. | 四种元素在自然界中均以化合态存在 |
16.下列离子方程式与实验事实相符且正确的是( )
| A. | 向AgI浊液中滴入NaCl溶液,产生大量白色沉淀:AgI(s)+Cl-(aq)=AgCl(s)+I-(aq) | |
| B. | 用氨水除去铝片表面的氧化膜:Al2O3+2NH3•H2O=2AlO2-+2NH4++H2O | |
| C. | 用铁氰化钾溶液检验Fe2+:3Fe2++2[Fe(CN)6]3-=Fe3[Fe(CN)6]2↓ | |
| D. | 向酸性KMnO4溶液中滴入过氧化氢产生无色气泡:2MnO4-+9H2O2+6H+=2Mn2++7O2↑+12H2O |
15.下列说法不正确的是( )
| A. | 开发利用太阳能与风能是发展低碳经济的重要途径 | |
| B. | 地沟油对人体危害严重,查证没收后应燃烧处理 | |
| C. | 氮化硅、碳化硅可做耐高温、耐磨材料 | |
| D. | 氯气、臭氧、高铁酸钾都是常用的自来水消毒剂 |
14.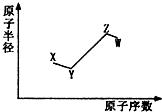 短周期非金属主族元素X、Y、Z、W,它们的原子半径与原子序数的关系如图所示.其中Z元素原子序数是Y的2倍,原子最外层电子数与X元素原子核外电子数相等,下列说法一定正确的是( )
短周期非金属主族元素X、Y、Z、W,它们的原子半径与原子序数的关系如图所示.其中Z元素原子序数是Y的2倍,原子最外层电子数与X元素原子核外电子数相等,下列说法一定正确的是( )
 短周期非金属主族元素X、Y、Z、W,它们的原子半径与原子序数的关系如图所示.其中Z元素原子序数是Y的2倍,原子最外层电子数与X元素原子核外电子数相等,下列说法一定正确的是( )
短周期非金属主族元素X、Y、Z、W,它们的原子半径与原子序数的关系如图所示.其中Z元素原子序数是Y的2倍,原子最外层电子数与X元素原子核外电子数相等,下列说法一定正确的是( )| A. | X和Z、Y和W处于同一主族 | |
| B. | 4种元素形成的各种单质中,Z单质的沸点最高 | |
| C. | W单质与X、Y、Z的最简单氢化物都可以发生反应 | |
| D. | 元素氧化物所对应的水化物酸性:W>Z>X |
13.下列离子组一定能大量共存的是( )
| A. | pH=1的无色溶液中:K+、NH4+、SO42-、MnO4- | |
| B. | 水电离出的c(OH-)=10-12 mo1•L-1的溶液中:Fe2+、Ba2+、NO3-、ClO- | |
| C. | 含大量A13+的溶液中:Na+、SO42-、NO3-、[Al(OH)4]- | |
| D. | CO2的饱和溶液中:K+、Ca2+、Cl-、NO3- |
11.下列说法中正确的是( )
0 167894 167902 167908 167912 167918 167920 167924 167930 167932 167938 167944 167948 167950 167954 167960 167962 167968 167972 167974 167978 167980 167984 167986 167988 167989 167990 167992 167993 167994 167996 167998 168002 168004 168008 168010 168014 168020 168022 168028 168032 168034 168038 168044 168050 168052 168058 168062 168064 168070 168074 168080 168088 203614
| A. | 同周期金属元素,原子失电子能力越强,最高化合价越高 | |
| B. | 同主族的单核阴离子,其还原性越强,水解程度越大 | |
| C. | IA和VIIA族元素间可形成共价化合物 | |
| D. | 第二周期元素从左到右最高化合价从+1到+7 |
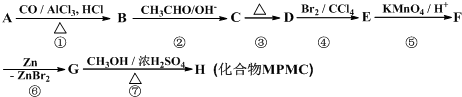
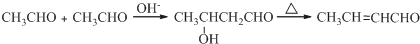
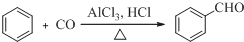
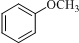 ;D
;D .
.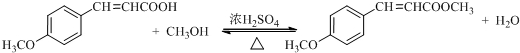 .
.
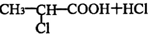
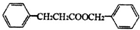 ;有机物M中含氧官能团名称是醛基.
;有机物M中含氧官能团名称是醛基. ,F→G
,F→G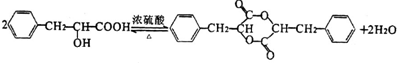 .
.