15.下列名称的有机物实际上不可能存在的是( )
| A. | 3,3-二甲基-2-戊烯 | B. | 2-甲基-4-乙基-1-己烯 | ||
| C. | 3-甲基-2-戊烯 | D. | 2,2-二甲基丁烷 |
12.某密闭容器中充入等物质的量的气体A和B,一定温度下发生如下反应:A(g)+xB(g)═2C(g),达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间的变化关系如图所示.下列说法中正确的是( )


| A. | 反应方程式中的x=1,30min时改变条件后,A的转化率将变减小 | |
| B. | 前30 min内 A的反应速率为0.05 mol/(L•min) | |
| C. | 20至40 min内表示处于平衡状态,该反应为放热反应 | |
| D. | 30 min时改变的条件是加入负催化剂,40 min时改变的条件是升高温度 |
11.有一处于平衡状态的反应:X(s)+3Y(g)═2Z(g)(正反应是放热反应).为了使平衡向生成Z的方向移动,应选择的条件是( )
①增加X ②降低温度 ③增大压强 ④降低压强 ⑤加入正催化剂 ⑥分离出Z.
①增加X ②降低温度 ③增大压强 ④降低压强 ⑤加入正催化剂 ⑥分离出Z.
| A. | ①③⑤ | B. | ②③⑥ | C. | ②③⑤ | D. | ②④⑥ |
10.在密闭容器中进行反应X2(g)+Y2(g)?2Z(g),已知X2、Y2、Z的起始浓度分别为0.1mol•L-1、0.2mol•L-1、0.1mol•L-1,在一定条件下,当反应达到平衡时,各物质的浓度有可能是( )
| A. | Y2为0.1 mol•L-1 | B. | X2为0.1 mol•L-1 | ||
| C. | Y2为0.35 mol•L-1 | D. | Z为0.3 mol•L-1 |
9.下列说法中正确的是( )
| A. | △H>0表示放热反应,△H<0表示吸热反应 | |
| B. | 反应产物的总焓大于反应物的总焓时,△H>0 | |
| C. | △H的大小与热化学方程式中的各物质的化学计量数无关 | |
| D. | 在化学反应中,发生物质变化的同时不一定发生能量变化 |
8.下列说法正确的是( )
0 167767 167775 167781 167785 167791 167793 167797 167803 167805 167811 167817 167821 167823 167827 167833 167835 167841 167845 167847 167851 167853 167857 167859 167861 167862 167863 167865 167866 167867 167869 167871 167875 167877 167881 167883 167887 167893 167895 167901 167905 167907 167911 167917 167923 167925 167931 167935 167937 167943 167947 167953 167961 203614
| A. | CO2的水溶液导电能力很弱,所以CO2是弱电解质 | |
| B. | 强电解质一定是易溶于水的化合物,弱电解质一定是难溶于水的化合物 | |
| C. | 在水溶液中能离解为自由移动的离子的化合物是电解质 | |
| D. | 在强电解质的水溶液中只有离子没有分子 |
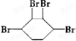
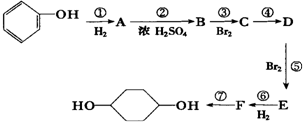 已知实验室由
已知实验室由 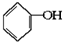 合成
合成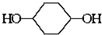 的反应流程如下 (部分试剂和反应条件已略去) (X代表卤素原子,R代表烃基)
的反应流程如下 (部分试剂和反应条件已略去) (X代表卤素原子,R代表烃基) 、D
、D
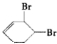 、
、
 合成氨是人类科学技术上的一项重大突破,其反应原理为:
合成氨是人类科学技术上的一项重大突破,其反应原理为: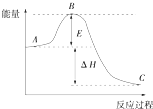 2SO2(g)+O2(g)═2SO3(g)反应过程的能量变化如图所示,已知1mol SO2(g) 被氧化为1mol SO3(g)的△H=-99kJ/mol.回答下列问题:
2SO2(g)+O2(g)═2SO3(g)反应过程的能量变化如图所示,已知1mol SO2(g) 被氧化为1mol SO3(g)的△H=-99kJ/mol.回答下列问题: