题目内容
10.在密闭容器中进行反应X2(g)+Y2(g)?2Z(g),已知X2、Y2、Z的起始浓度分别为0.1mol•L-1、0.2mol•L-1、0.1mol•L-1,在一定条件下,当反应达到平衡时,各物质的浓度有可能是( )| A. | Y2为0.1 mol•L-1 | B. | X2为0.1 mol•L-1 | ||
| C. | Y2为0.35 mol•L-1 | D. | Z为0.3 mol•L-1 |
分析 在一定条件下,该反应可能向正反应方向进行也可能向逆反应方向进行,采用极限方法判断平衡时各物质浓度,如果平衡向正反应方向进行,反应物X2完全转化为Z,则Z最大、X2和Y2的浓度最小,如果平衡向逆反应方向进行,Z完全转化为生成物X2和Y2,则X2和Y2最大、Z最小,实际上该反应存在平衡状态,所以平衡时各物质浓度介于最大和最小之间,据此分析解答.
解答 解:如果平衡向正反应方向进行,反应物X2完全转化为Z,则Z最大、X2和Y2的浓度最小,根据方程式知,生成Z为0.2mol•L-1,消耗Y20.1mol•L-1,则X2最小为0、Y2最小为0.1mol•L-1、Z为0.3mol•L-1;如果平衡向逆反应方向进行,Z完全转化为X2和Y2,则X2和Y2最大、Z最小,X2为0.15mol•L-1、Y2为0.25mol•L-1,Z为0;
实际上该反应存在平衡状态,所以平衡时各物质浓度介于最大和最小之间,X2浓度在0-0.15mol•L-1之间、Y2浓度在0.1mol•L-1-0.25mol•L-1之间、Z浓度在0-0.3mol•L-1之间
A.平衡时Y2浓度在0.1mol•L-1-0.25mol•L-1之间,故A错误;
B.平衡时X2浓度在0-0.15mol•L-1之间,故B正确;
C.平衡时Y2浓度在0.1mol•L-1-0.25mol•L-1之间,故C错误;
D.平衡时Z浓度在0-0.3mol•L-1之间,故D错误;
故选B.
点评 本题考查化学平衡建立过程,侧重考查学生分析判断及计算能力,采用极限法分析解答即可,题目难度不大.

练习册系列答案
相关题目
15.下列名称的有机物实际上不可能存在的是( )
| A. | 3,3-二甲基-2-戊烯 | B. | 2-甲基-4-乙基-1-己烯 | ||
| C. | 3-甲基-2-戊烯 | D. | 2,2-二甲基丁烷 |
2.分子式为C3H4Cl2的链状有机物的同分异构体共有(不包括立体异构)( )
| A. | 6种 | B. | 5种 | C. | 4种 | D. | 3种 |
20.某化学课外学习小组对元素周期律和元素周期表进行研究和探讨,一部分同学提出了下列看法,你认为不正确的是( )
| A. | 原子的最外层有两个电子的元素并不都在第ⅡA族 | |
| B. | 第ⅠA族元素都是典型的金属元素 | |
| C. | 第ⅦA族的元素最外层都有七个电子 | |
| D. | 第三周期的元素的原子核外都有三个电子层 |
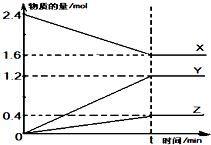 在2L容器中有3种物质进行反应,X、Y、Z的物质的量随时间的变化曲线如图所示,反应在t时刻达到平衡.
在2L容器中有3种物质进行反应,X、Y、Z的物质的量随时间的变化曲线如图所示,反应在t时刻达到平衡.