16.几种短周期元素的原子半径及主要化合价见下表
根据表中信息,判断以下说法正确的是( )
| 元素符号 | X | Y | Z | R | T |
| 原子半径(nm) | 0.160 | 0.080 | 0.102 | 0.143 | 0.074 |
| 主要化合价 | +2 | +2 | -2,+4,+6 | +3 | -2 |
| A. | 单质与稀硫酸反应的速率快慢:R>X>Y | |
| B. | 离子半径:T2->X2+ | |
| C. | 元素最高价氧化物的水化物的碱性:X>R>Y | |
| D. | 单质与氢气化合的难易程度:Z>T |
15.下表是部分短周期元素的原子半径及主要化合价,根据表中信息判断正确的是( )
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.089 | 0.102 | 0.074 |
| 主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
| A. | L2+与R2-的核外电子数相等 | |
| B. | M与T形成的化合物既能与强酸反应又能与强碱反应 | |
| C. | 氢化物的沸点为H2T>H2R | |
| D. | 单质与浓度相等的稀盐酸反应的剧烈程度为Q>L |
14.下列有关叙述中不正确的是( )
| A. | 相同温度下,0.02 mol•L-1的醋酸溶液与0.01 mol•L-1的醋酸溶液中的c(H+)之比小于2:1 | |
| B. | 相同温度下,0.1 mol•L-1 (NH4)2SO4溶液与0.1 mol•L-1NH4NO3溶液中c(NH4+)之比大于2:1 | |
| C. | 在0.1 mol•L-1NaOH溶液中逐滴加入0.1 mol•L-1CH3COOH溶液,当溶液pH=7时,加入CH3COOH溶液的体积与NaOH溶液的体积比小于2:1 | |
| D. | 40℃时,pH=7的(NH4)2SO4与NH3•H2O的混合溶液中c(NH4+)与c(SO42-)之比小于2:1 |
13.分子式为C6H12O2,属于乙酸乙酯同系物的同分异构体共有( )
| A. | 12种 | B. | 16种 | C. | 20种 | D. | 24种 |
12.下列方程式表示的反应既不属于加成反应也不属于取代反应的是( )
| A. | C6H5CH2Cl+NaCN→C6H5CH2CN+NaCl | |
| B. | C6H5Li+CO2→C6H5COOLi | |
| C. | CH3CH2CHO+HCN$\stackrel{NaOH}{→}$ | |
| D. | CH3COOCH2CH3$→_{气相}^{450℃}$CH3COOH+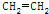 |
11.乙醇分子结构中的各种化学键如下图所示,下列关于乙醇在各种反应中断键的说法,正确的是( )

| A. | 与醋酸、浓硫酸共热时断裂① | |
| B. | 在浓硫酸存在下加热至170℃时断裂②⑤ | |
| C. | 和金属钠反应时断裂② | |
| D. | 在Cu催化下和O2反应时断裂②③ |
10.下列操作达不到预期目的是( )
①石油分馏时把温度计插入液面以下;②用溴水除去乙烯中混有的SO2气体;③用乙醇与3mol/L的H2SO4混合共热到170℃制取乙烯;④将苯和溴水混合后加入Fe粉制溴苯;⑤将饱和食盐水滴入盛有电石的烧瓶中制乙炔.
①石油分馏时把温度计插入液面以下;②用溴水除去乙烯中混有的SO2气体;③用乙醇与3mol/L的H2SO4混合共热到170℃制取乙烯;④将苯和溴水混合后加入Fe粉制溴苯;⑤将饱和食盐水滴入盛有电石的烧瓶中制乙炔.
| A. | ①④ | B. | ③⑤ | C. | ②③④⑤ | D. | ①②③④ |
9.能发生消去反应,且生成物中存在同分异构体的是( )
0 167738 167746 167752 167756 167762 167764 167768 167774 167776 167782 167788 167792 167794 167798 167804 167806 167812 167816 167818 167822 167824 167828 167830 167832 167833 167834 167836 167837 167838 167840 167842 167846 167848 167852 167854 167858 167864 167866 167872 167876 167878 167882 167888 167894 167896 167902 167906 167908 167914 167918 167924 167932 203614
| A. | 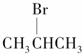 | B. |  | C. |  | D. | CH3Cl |
 ,推测苯分子中有两种不同的碳碳键,即碳碳单键和碳碳双键,因此它可以使紫色的高锰酸钾溶液褪色.
,推测苯分子中有两种不同的碳碳键,即碳碳单键和碳碳双键,因此它可以使紫色的高锰酸钾溶液褪色.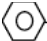 表示苯分子的结构更合理.
表示苯分子的结构更合理.