12.下列说法正确的是( )
| A. | 所有主族元素的最高正化合价都等于其最外层电子数 | |
| B. | 所有过渡元素都是金属元素,所有的金属元素也都是过渡元素 | |
| C. | 在周期表中氧族元素的单质全部是气体 | |
| D. | 同周期主族元素的原子半径以ⅦA族的为最小 |
11.下列哪组离子能在水溶液中大量共存( )
| A. | K+、CO32-、HS-、S2-、Al3+、AlO2- | B. | MnO4-、Na+、SO42-、K+、Cl- | ||
| C. | SO42-、Ag+、SO32-、S2-、AlO2-、K+ | D. | Fe3+、Cl-、H+、NO3- |
9.下列说法中,正确的是( )
| A. | 中和反应反应热的测定实验中,将环形玻璃搅拌棒换成环形铜丝搅拌棒测定出来的中和热值偏大 | |
| B. | 在101kPa时,2gH2完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)═2H2O(l)△H=-571.6KJ/mol | |
| C. | 将0.5molN2和1.5molH2置于密闭容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g)?2NH3(g)△H=-38.6KJ/mol | |
| D. | HCl和NaOH反应的中和热△H=-57.3KJ/mol,则H2SO4和Ca(OH)2反应的反应热△H=-(2×57.3)KJ/mol |
6.已知t℃时AgCl的Ksp=2×10-10;Ag2CrO4是一种橙红色固体,t℃时,在水中的沉淀溶解平衡曲线如图所示.下列说法正确的是( )
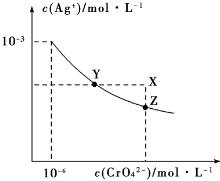

| A. | 在t℃时,Ag2CrO4的Ksp为1×10-12 | |
| B. | 在t℃时,AgCl的溶解度大于Ag2CrO4 | |
| C. | 在饱和Ag2CrO4溶液中加入K2CrO4,可使溶液由Y点到X点 | |
| D. | 在t℃时,用AgNO3标准溶液滴定20mL未知浓度的KCl溶液,不能采用K2CrO4溶液为指示剂 |
5.短周期主要元素X、Y、Z、W的原子序列数依次增大,X原子核外最外层电子数是次外层的2倍,Y的氯化物YF3,分子中各原子均达到8电子稳定结构,Z是同周期中原子半径最大的元素,W的最高正价为+7价,下列说法正确的是( )
| A. | 简单离子半径的大小顺序为:rw>rz>ry | |
| B. | 元素W的氧化物对应水化物的酸性比Y的强 | |
| C. | X与Y形成的晶体XaYa的熔点高硬度大,为可替代金刚石的材料 | |
| D. | X与W形成的化合物和Z与W形成的化合物的化学类型相同 |
4.中学化学中很多“规律”都有其适用范围,下列根据有关“规律”推出的结论正确的是( )
0 167354 167362 167368 167372 167378 167380 167384 167390 167392 167398 167404 167408 167410 167414 167420 167422 167428 167432 167434 167438 167440 167444 167446 167448 167449 167450 167452 167453 167454 167456 167458 167462 167464 167468 167470 167474 167480 167482 167488 167492 167494 167498 167504 167510 167512 167518 167522 167524 167530 167534 167540 167548 203614
| 选项 | 规律 | 结论 |
| A | 强氧化性物质可以用来杀菌消毒 | ClO2可用于自来水消毒 |
| B | 反应物浓度越大,反应速率越快 | 常温下,相同的铝片中分别加入足量的浓、稀硫酸,浓硫酸中铝片先溶解完 |
| C | 结构和组成相似的物质,沸点随相对分子质量增大而升高 | NH3沸点低于PH3 |
| D | 较强的酸可以制取较弱的酸 | 硫化氢通入硫酸铜溶液中不能反应 |
| A. | A | B. | B | C. | C | D. | D |
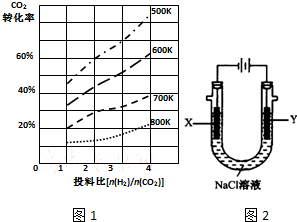 研究CO2的利用对促进低碳社会的构建具有重要的意义.
研究CO2的利用对促进低碳社会的构建具有重要的意义.