4.下列关于化学的叙述中,错误的是( )
| A. | 在化工生产中应遵循“绿色化学”的思想 | |
| B. | 通常用来衡量一个国家的石油化学工业发展水平的标志是乙烯的产量 | |
| C. | 在元素周期表的金属和非金属分界线附近寻找半导体材料 | |
| D. | 根据元素周期律,由HClO4可以类推出氟元素也存在最高价氧化物的水化物HFO4 |
3.下列说法正确的是( )
| A. | 所有碳原子间只以单键相连的链烃是烷烃 | |
| B. | 所有糖类物质都有甜味 | |
| C. | 糖类、油脂、蛋白质都能水解 | |
| D. | 葡萄糖与蔗糖互为同分异构体 |
20.某有机物结构如下:CH3-CH=CH-Cl,该有机物能发生:①取代反应 ②加成反应 ③聚合反应 ④使溴水褪色 ⑤使酸性KMnO4溶液褪色 ⑥AgNO3溶液生成白色沉淀( )
| A. | 以上反应均可发生 | B. | 只有①不能发生 | ||
| C. | 只有⑥不能发生 | D. | 只有②不能发生 |
19.下列说法正确的是( )
| A. | 分子式相同的不同物质一定是同分异构体 | |
| B. | 通式相同的不同物质一定属于同系物 | |
| C. | 相对分子质量相同的不同物质一定是同分异构体 | |
| D. | 分子式相同,元素的质量分数也相同的物质是同种物质 |
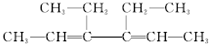
18.某烃含碳、氢元素的质量比为6:1,该径对氮气的相对密度为2,它即可使溴水褪色,又能与氢气加成,而与氢气的加成产物的有3种同分异构体,该径可以是( )
| A. | H2C=CH-CH2-CH3 | B. | 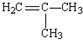 | C. | H2C=CH2 | D. | 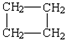 |
17.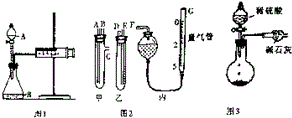 某校化学小组的同学开展测定Na2CO3和NaCl的固体混合物中Na2CO3质量分数的探究实验,他们提出下列实验方案-气体分析法.
某校化学小组的同学开展测定Na2CO3和NaCl的固体混合物中Na2CO3质量分数的探究实验,他们提出下列实验方案-气体分析法.
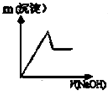
(1)甲同学用图1所示装置,把Ng的混合物与足量稀硫酸反应后,测定产生的CO2气体的体积,实验开始时检查该装置气密性的方法是关闭A处活塞,将注射器活塞拉出一定距离,一段时间后松开活塞,若活塞能回到原位,证明不漏气,否则漏气.
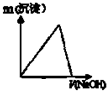
(2)乙同学用图2代替图1中的发生、收集装置,甲、乙两试管各有两根导管,用橡胶管连接对应接口后,倒置盛有稀硫酸的试管,发生反应,放出气体,则Na2CO3、NaCl的固体混合物和稀硫酸应分别置于甲、乙仪器中(填仪器编号);G管可用化学实验室里的一种常用仪器来代替,你认为这种仪器的名称是碱式滴定管;仪器甲、乙、丙接口的连接方式如下:A连接D,B连接E,C连接F(填写各接口的编号).
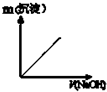
(3)丙同学用图3装置测定CO2的质量,该装置存在明显缺陷,从而导致实验误差,请你分析其中使测定结果可能偏大的主要原因CO2气体中混有水蒸气或空气中的CO2和水蒸气进入干燥管中,使测定结果可能偏小的主要原因可能是装置中的CO2没有全部被碱石灰吸收;(上述偏大、偏小的原因各写一条)
(4)某天然碱可看作向CO2和NaOH的反应后的产物所组成,称取天碱样品四份,溶于水后,分别逐滴加入相同浓度的盐酸溶液30毫升,产生CO2的体积(标准状况)如下表:
取3.28g天然碱样品于300℃加热至分解完全(300℃Na2CO3不分解),产生CO2224mL(标准状况)和一定量的水,则该天然碱样品的化学式为Na2CO3•2NaHO3•3H2O.
 某校化学小组的同学开展测定Na2CO3和NaCl的固体混合物中Na2CO3质量分数的探究实验,他们提出下列实验方案-气体分析法.
某校化学小组的同学开展测定Na2CO3和NaCl的固体混合物中Na2CO3质量分数的探究实验,他们提出下列实验方案-气体分析法.(1)甲同学用图1所示装置,把Ng的混合物与足量稀硫酸反应后,测定产生的CO2气体的体积,实验开始时检查该装置气密性的方法是关闭A处活塞,将注射器活塞拉出一定距离,一段时间后松开活塞,若活塞能回到原位,证明不漏气,否则漏气.
(2)乙同学用图2代替图1中的发生、收集装置,甲、乙两试管各有两根导管,用橡胶管连接对应接口后,倒置盛有稀硫酸的试管,发生反应,放出气体,则Na2CO3、NaCl的固体混合物和稀硫酸应分别置于甲、乙仪器中(填仪器编号);G管可用化学实验室里的一种常用仪器来代替,你认为这种仪器的名称是碱式滴定管;仪器甲、乙、丙接口的连接方式如下:A连接D,B连接E,C连接F(填写各接口的编号).
(3)丙同学用图3装置测定CO2的质量,该装置存在明显缺陷,从而导致实验误差,请你分析其中使测定结果可能偏大的主要原因CO2气体中混有水蒸气或空气中的CO2和水蒸气进入干燥管中,使测定结果可能偏小的主要原因可能是装置中的CO2没有全部被碱石灰吸收;(上述偏大、偏小的原因各写一条)
(4)某天然碱可看作向CO2和NaOH的反应后的产物所组成,称取天碱样品四份,溶于水后,分别逐滴加入相同浓度的盐酸溶液30毫升,产生CO2的体积(标准状况)如下表:
| 样品号 | Ⅰ | Ⅱ | Ⅲ | Ⅳ |
| 盐酸溶液的体积/mL | 30 | 30 | 30 | 30 |
| 样品质量/g | 3.32 | 4.15 | 5.81 | 7.47 |
| 二氧化碳的体积/mL | 672 | 840 | 896 | 672 |
16.二甲醛是一种重要的化工原料,利用水煤气(CO、H2)合成二甲醛是工业上的常用方法,该方法由以下几步组成:

2H2(g)+CO(g)?CH3OH(g)△H=-90.0kJ•mol-1 ①
2CH3OH(g)?CH3OCH3(g)△H=-24.5kJ•mol-1 ②
CO(g)+H2O(g)?CO2(g)+H2(g)△H=-41.1mol kJ•mol-1 ③
(1)反应①的△S<0(填“>”“<”或“=”),在较低(填“较高”或“较低”)温度下该反应自发进行.
(2)在250℃的恒容密闭容器中,下列事实可以作为反应③已达平衡的是BC(填选项字母).
A.容器内气体密度保持不变
B.CO与CO2的物质的量之比保持不变
C.H2O与CO2的生成速率之比为1:1
D.该反应的平衡常数保持不变
(3)已知一些共价键的键能如下:
运用反应①计算一氧化碳中碳氧共价键的键能1070kJ•mol-1.
(4)当合成气体中CO与H2的物质的量之比恒定时,温度、压强CO转化率的影响如图1所示.图1中A点的v(逆)<B点的v(正)(填“>”“<”或“=”).说明理由B点对应的温度和压强都比A点高,温度升高,或压强增大,都会加快反应速率.实际工业生产中该合成反应的条件为500℃、4MPa,请回答采用500℃的可能原因500℃时一氧化碳转化率较大,反应速率也较快.若温度过高,一氧化碳转化率降低,若温度过低,反应速率太慢.
(5)一定温度下,密闭容器中发生反应③,水蒸气的转化率与a(H2O)/h(CO)的关系如图2所示,计算该温度下发生反应③的平衡常数K=1.
在图2中作出一氧化碳的转化率n(H2O)/n(CO)的曲线.
0 167266 167274 167280 167284 167290 167292 167296 167302 167304 167310 167316 167320 167322 167326 167332 167334 167340 167344 167346 167350 167352 167356 167358 167360 167361 167362 167364 167365 167366 167368 167370 167374 167376 167380 167382 167386 167392 167394 167400 167404 167406 167410 167416 167422 167424 167430 167434 167436 167442 167446 167452 167460 203614

2H2(g)+CO(g)?CH3OH(g)△H=-90.0kJ•mol-1 ①
2CH3OH(g)?CH3OCH3(g)△H=-24.5kJ•mol-1 ②
CO(g)+H2O(g)?CO2(g)+H2(g)△H=-41.1mol kJ•mol-1 ③
(1)反应①的△S<0(填“>”“<”或“=”),在较低(填“较高”或“较低”)温度下该反应自发进行.
(2)在250℃的恒容密闭容器中,下列事实可以作为反应③已达平衡的是BC(填选项字母).
A.容器内气体密度保持不变
B.CO与CO2的物质的量之比保持不变
C.H2O与CO2的生成速率之比为1:1
D.该反应的平衡常数保持不变
(3)已知一些共价键的键能如下:
| 共价键 | H-H | C-H | C-O | O-H |
| 键能(kJ-mol-3) | 436 | 414 | 326 | 464 |
(4)当合成气体中CO与H2的物质的量之比恒定时,温度、压强CO转化率的影响如图1所示.图1中A点的v(逆)<B点的v(正)(填“>”“<”或“=”).说明理由B点对应的温度和压强都比A点高,温度升高,或压强增大,都会加快反应速率.实际工业生产中该合成反应的条件为500℃、4MPa,请回答采用500℃的可能原因500℃时一氧化碳转化率较大,反应速率也较快.若温度过高,一氧化碳转化率降低,若温度过低,反应速率太慢.
(5)一定温度下,密闭容器中发生反应③,水蒸气的转化率与a(H2O)/h(CO)的关系如图2所示,计算该温度下发生反应③的平衡常数K=1.
在图2中作出一氧化碳的转化率n(H2O)/n(CO)的曲线.