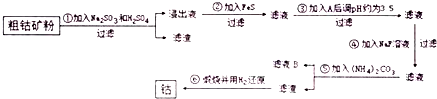
15.化学与人类生活、环境保护及社会可持续发展密切相关,下列有关叙述正确的是( )
| A. | 大量开发利用深海可燃冰,有助于海洋生态环境的治理 | |
| B. | 汽车尾气中含有大量大气污染物,其原因是汽油不完全燃烧造成的 | |
| C. | 煤炭燃烧过程安装固硫装置,目的是提高煤的利用率 | |
| D. | PM2.5表面积大,能吸附大量的有毒有害物质,对人的肺功能造成很大危害 |
14.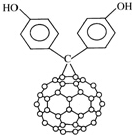 由于C60具有碳碳双键所以又名为“足球烯”;C60的二苯酚基化合物结构如图.下列关于C60的二苯酚基化合物的叙述正确的是( )
由于C60具有碳碳双键所以又名为“足球烯”;C60的二苯酚基化合物结构如图.下列关于C60的二苯酚基化合物的叙述正确的是( )
 由于C60具有碳碳双键所以又名为“足球烯”;C60的二苯酚基化合物结构如图.下列关于C60的二苯酚基化合物的叙述正确的是( )
由于C60具有碳碳双键所以又名为“足球烯”;C60的二苯酚基化合物结构如图.下列关于C60的二苯酚基化合物的叙述正确的是( )| A. | C60的二苯酚基化合物属于芳香烃 | |
| B. | C60的二苯酚基化合物分子式为C73H12O2 | |
| C. | C60的二苯酚基化合物能与氢氧化钠溶液反应 | |
| D. | 1mol C60的二苯酚基化合物最多可以与6mol H2发生加成反应 |
12.日常用牙膏的主要成分有:活性物质,摩擦剂,甘油等,假设牙膏中的摩擦剂成分为CaC03、SiO2、Al(OH)3中的一种或几种物质组成,牙膏中其他成分均可溶于盐酸,且无气体产生.
(1)牙膏中添加甘油主要作用保温
为进一步炭疽牙膏中摩擦剂成分,进行了以下探究:
Ⅰ.摩擦剂成分的定性检验:
设计实验方案,验证假设,请写出实验步骤以及预期现象和结论(可不填满也可补充).可选的试剂:稀盐酸,稀硫酸,NaOH溶液,澄清石灰水.
Ⅱ.牙膏样品中碳酸钙的定量测定
利用如图所示装置(图中夹持仪器略去)进行实验,充分反应后,测定C中生成的BaCO3沉淀质量,以确定碳酸钙的质量分数

依据实验过程回答下列问题
(2)实验过程中需持续缓缓通入空气,其主要作用将生成的二氧化碳全部排入C中,使之完全被氢氧化钡吸收
(3)仪器C中选择Ba(OH)2而不选择Ca(OH)2溶液原因:①氢氧化钡的溶解度大,可以配制得较高的浓度②产物碳酸钡的相对分子量大,可以减小实验误差
(4)下列各项措施中,能提高测定准确经度的是ab(填标号)
a.在加入盐酸之前,应排净装置内的CO2气体
b.缓慢滴加稀盐酸
c.在A-B之间增添盛有浓硫酸的洗气装置
d.在B-C之间增添盛有饱和碳酸氢钠溶液的洗气装置
(5)实验中准确称取1.00g样品三份,进行三次测定,测得BaCO2平均质量为3.94g,测样品中碳酸钙的质量分数为20%,若改测定C中生成BaCO2的质量分数,两方法测定的结果不同(填“相同”或“不同”),原因是B中的水蒸气、氯化氢气体等进入装置C中.
(1)牙膏中添加甘油主要作用保温
为进一步炭疽牙膏中摩擦剂成分,进行了以下探究:
Ⅰ.摩擦剂成分的定性检验:
设计实验方案,验证假设,请写出实验步骤以及预期现象和结论(可不填满也可补充).可选的试剂:稀盐酸,稀硫酸,NaOH溶液,澄清石灰水.
| 实验步骤 | 预期现象和结论 |
| 步骤1:取适量牙膏样品,加水充分搅拌、过滤 | 有难溶物存在 |
| 步骤2: | ①有无色气泡产生,说明有CaCO3 ②出现无色气泡,说明含有碳酸钙,说明有若有难溶物存在,说明有二氧化硅 |
| 步骤3: | |
| … |
利用如图所示装置(图中夹持仪器略去)进行实验,充分反应后,测定C中生成的BaCO3沉淀质量,以确定碳酸钙的质量分数

依据实验过程回答下列问题
(2)实验过程中需持续缓缓通入空气,其主要作用将生成的二氧化碳全部排入C中,使之完全被氢氧化钡吸收
(3)仪器C中选择Ba(OH)2而不选择Ca(OH)2溶液原因:①氢氧化钡的溶解度大,可以配制得较高的浓度②产物碳酸钡的相对分子量大,可以减小实验误差
(4)下列各项措施中,能提高测定准确经度的是ab(填标号)
a.在加入盐酸之前,应排净装置内的CO2气体
b.缓慢滴加稀盐酸
c.在A-B之间增添盛有浓硫酸的洗气装置
d.在B-C之间增添盛有饱和碳酸氢钠溶液的洗气装置
(5)实验中准确称取1.00g样品三份,进行三次测定,测得BaCO2平均质量为3.94g,测样品中碳酸钙的质量分数为20%,若改测定C中生成BaCO2的质量分数,两方法测定的结果不同(填“相同”或“不同”),原因是B中的水蒸气、氯化氢气体等进入装置C中.
10.已知NaHSO2溶液在不同温度下均可被过量KlO3氧化,当NaHSO3完全消耗即有I2析出,依据I2析出所需时间可以求得NaHSO3的反应速率.将浓度均为0.020 mol•L-1的NaHSO3溶液(含少量淀粉)10.0 mL、KIO3(过量)酸性溶液40.0 mL混合,记录10~55℃间溶液变蓝时间,55℃时未观察到溶液变蓝,实验结果如图.据图分析,下列判断不正确的是( )
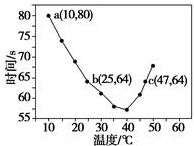

| A. | 40℃之前与40℃之后溶液变蓝的时间随温度的变化趋势相反 | |
| B. | 图中a点对应的NaHSO3反应速率为5.0×10-5 mol•L-1•s-1 | |
| C. | 图中b、c两点对应的NaHSO3反应速率相等 | |
| D. | 40℃之后,淀粉不宜用作该实验的指示剂 |
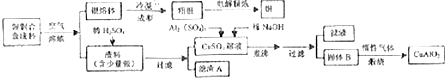
9.电解Na2SO4溶液产生H2SO4和烧碱的装置如图所示,其中阴极和阳极均为惰性电极.测得同温同压下,气体甲与气体乙的体积比约为1:2,以下说法正确的是(说明:阳离子交换膜只允许阳离子通过,阴离子交换膜只允许阴离子通过)( )
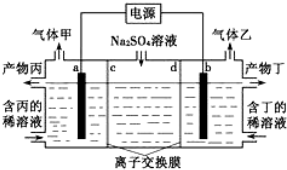

| A. | a电极反应式:2H++2e-=H2↑ | |
| B. | 产物丁为NaOH | |
| C. | c为阳离子交换膜 | |
| D. | 每转移0.2mol电子,产生1.12L气体甲 |
7.某元素最高价氧化物对应水化物的化学式是H2XO3,这种元素的气态氢化物的分子式为( )
| A. | HX | B. | H2X | C. | XH3 | D. | XH4 |
6.下列有关叙述:①非金属M从化合物中置换出非金属单质N;
②M原子比N原子容易得到电子;
③单质M跟H2反应比N跟H2反应容易得多;
④气态氢化物水溶液的酸性HmM>HnN;
⑤氧化物水化物的酸性HmMOx>HnNOy;
⑥熔点M>N.
能说明非金属元素M比N的非金属性强的是( )
0 167054 167062 167068 167072 167078 167080 167084 167090 167092 167098 167104 167108 167110 167114 167120 167122 167128 167132 167134 167138 167140 167144 167146 167148 167149 167150 167152 167153 167154 167156 167158 167162 167164 167168 167170 167174 167180 167182 167188 167192 167194 167198 167204 167210 167212 167218 167222 167224 167230 167234 167240 167248 203614
②M原子比N原子容易得到电子;
③单质M跟H2反应比N跟H2反应容易得多;
④气态氢化物水溶液的酸性HmM>HnN;
⑤氧化物水化物的酸性HmMOx>HnNOy;
⑥熔点M>N.
能说明非金属元素M比N的非金属性强的是( )
| A. | ②⑤ | B. | ①②③ | C. | ①②③⑤ | D. | 全部 |