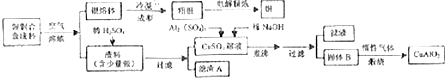
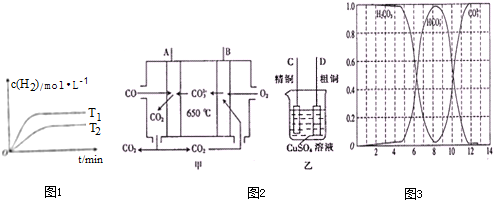
题目内容
6.下列有关叙述:①非金属M从化合物中置换出非金属单质N;②M原子比N原子容易得到电子;
③单质M跟H2反应比N跟H2反应容易得多;
④气态氢化物水溶液的酸性HmM>HnN;
⑤氧化物水化物的酸性HmMOx>HnNOy;
⑥熔点M>N.
能说明非金属元素M比N的非金属性强的是( )
| A. | ②⑤ | B. | ①②③ | C. | ①②③⑤ | D. | 全部 |
分析 比较元素的非金属性强弱,可从与氢气反应的剧烈程度、氢化物的稳定性、最高价氧化物对应水化物的酸性强弱等角度判断,注意不能根据得失电子的多少以及熔沸点的高低等角度判断.
解答 解:①非金属单质M能从N的化合物中置换出非金属单质N,可说明M比N的非金属性强,故①正确;
②M原子比N原子容易得到电子,可说明M比N的非金属性强,故②正确;
③单质M跟H2反应比N跟H2反应容易得多,则M易得电子,所以M比N的非金属性强,故③正确;
④不能利用氢化物的水溶液的酸性比较非金属性的强弱,故④错误;
⑤氧化物水化物的酸性HmMOx>HnNOy,不一定为最高价氧化物对应的水化物的酸性,则不能说明M、N的非金属性强弱,故⑤错误;
⑥M的单质熔点比N的高,属于物理性质,与得失电子的能力无关,不能用来判断非金属性的强弱,故⑥错误.
正确的有①②③,故选B.
点评 本题考查非金属性的比较,题目难度不大,本题注意把握比较非金属性的角度,注意元素周期律的变化.

练习册系列答案
相关题目
17.在有机物分子中,若碳原子连接四个不同的原子或原子团,该碳原子称为手性碳原子,以*C表示.具有手性碳原子的有机物具有光学活性.下列分子中,没有光学活性的是( )
| A. | 乳酸:CH3-CH(OH)-COOH | |
| B. | 甘油:CH2(OH)-CH(OH)-CH2(OH) | |
| C. | 脱氧核糖:CH2(OH)-CH(OH)-CH(OH)-CH2-CHO | |
| D. | 核糖:CH2(OH)-CH(OH)-CH(OH)-CH(OH)-CHO |
14.1996年2月9 日欧洲一科学小组,由${\;}_{30}^{60}$Zn和${\;}_{82}^{208}$Pb两原子经核聚合,并放出一定数目的中子而制得${\;}_{112}^{227}$X原子,则两原子在核聚合过程中放出的中子数目是( )
| A. | 41 | B. | 115 | C. | 142 | D. | 162 |
1.下列说法中,正确的是( )
| A. | 治理“地沟油”,可通过水解反应制得肥皂 | |
| B. | 硅晶体具有半导体性能,可用于制取光导纤维 | |
| C. | 人类超量碳排放及氮氧化物和二氧化硫的排放是形成酸雨的主要原因 | |
| D. | PM2.5是指空气中直径≤2.5 μm的颗粒物,直径为2.5 μm的颗粒物分散在空气中形成胶体(1μm=10-6m) |
18.下列离子方程式中,正确的是( )
| A. | Fe3O4溶于足量稀HNO3:Fe3O4+8H+=Fe2++2Fe3++4H2O | |
| B. | 硅酸钠溶液与醋酸溶液混合:SiO32-+2H+=H2SiO3↓ | |
| C. | AlCl3溶液中加入过量的氨水:Al3++4OH-=AlO2-+2H2O | |
| D. | 向NaHCO3溶液中加入过量Ca(OH)2溶液:HCO3-+Ca2++OH-=CaCO3↓+H2O |
15.下列粒子中,其最外层与最里层的电子数之和等于次外层电子数的是( )
| A. | S | B. | Mg | C. | Cl | D. | Be |
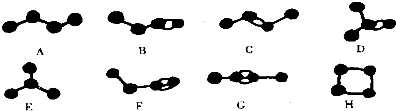
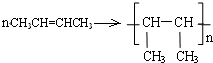 .
.