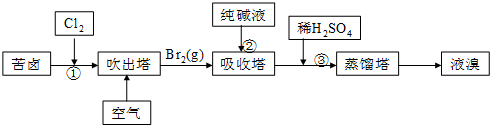
5.Cl2、漂白液(有效成分为NaClO)在生产、生活中广泛用于杀菌、消毒.
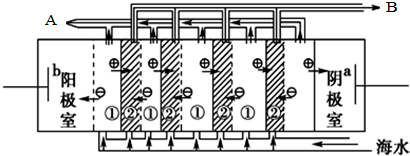
(1)电解NaCl溶液生成Cl2的化学方程式是2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑
(2)①Cl2溶于H2O、NaOH溶液即获得氯水、漂白液.
干燥的氯气不能漂白物质,但氯水却有漂白作用,说明起漂白作用的物质是HClO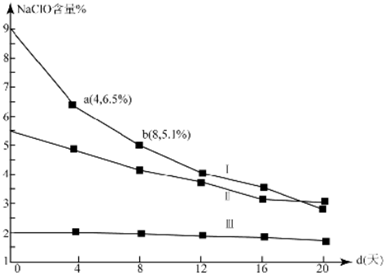
②25℃,Cl2与H2O、NaOH的反应如下:
不直接使用氯水而使用漂白液做消毒剂的原因是K2>K1,反应Ⅱ的有效成分比反应Ⅰ的有效成分大,氯气转化为HClO更充分,次氯酸钠比次氯酸更稳定
(3)家庭使用漂白液时,不宜直接接触铁制品,漂白液腐蚀铁的电极反应为:Fe-2e-=Fe2+:ClO-发生的电极反应式是ClO-+2e-+H2O=Cl-+2OH-
(4)研究漂白液的稳定性对其生产和保存有实际意义.30℃时,pH=11的漂白液中NaClO的质量百分含量随时间变化如下:
①分解速v(Ⅰ)、v(Ⅱ)的大小关系是>,原因是在相同条件下,次氯酸钠的浓度越大,其分解速率越大
②NaClO分解的化学方程式是2NaClO$\frac{\underline{\;30℃\;}}{\;}$2NaCl+O2↑
③4d~8d,Ⅰ中v(NaClO)=0.047mol/(L.d)(常温下漂白液的密度约为1g/cm3,且变化忽略不计)
0 166946 166954 166960 166964 166970 166972 166976 166982 166984 166990 166996 167000 167002 167006 167012 167014 167020 167024 167026 167030 167032 167036 167038 167040 167041 167042 167044 167045 167046 167048 167050 167054 167056 167060 167062 167066 167072 167074 167080 167084 167086 167090 167096 167102 167104 167110 167114 167116 167122 167126 167132 167140 203614
(1)电解NaCl溶液生成Cl2的化学方程式是2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑
(2)①Cl2溶于H2O、NaOH溶液即获得氯水、漂白液.
干燥的氯气不能漂白物质,但氯水却有漂白作用,说明起漂白作用的物质是HClO

②25℃,Cl2与H2O、NaOH的反应如下:
| 反应Ⅰ | Cl2+H2O?Cl-+H++HClO K1=4.5×10-4 |
| 反应Ⅱ | Cl2+2OH-?Cl-+ClO-+H2O K2=7.5×1015 |
(3)家庭使用漂白液时,不宜直接接触铁制品,漂白液腐蚀铁的电极反应为:Fe-2e-=Fe2+:ClO-发生的电极反应式是ClO-+2e-+H2O=Cl-+2OH-
(4)研究漂白液的稳定性对其生产和保存有实际意义.30℃时,pH=11的漂白液中NaClO的质量百分含量随时间变化如下:
①分解速v(Ⅰ)、v(Ⅱ)的大小关系是>,原因是在相同条件下,次氯酸钠的浓度越大,其分解速率越大
②NaClO分解的化学方程式是2NaClO$\frac{\underline{\;30℃\;}}{\;}$2NaCl+O2↑
③4d~8d,Ⅰ中v(NaClO)=0.047mol/(L.d)(常温下漂白液的密度约为1g/cm3,且变化忽略不计)
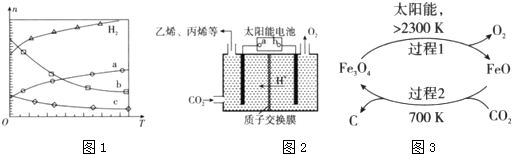
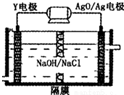 短周期元素X、Y、Z、W原子序数依次增大,X氢化物的水溶液显碱性;Y在元素周期表中所处的周期序数与族序数相等;Z单质是将太阳能转化为电能的常用材料;W是重要的“成盐元素”,主要以钠盐的形式存在于海水中,请回答:
短周期元素X、Y、Z、W原子序数依次增大,X氢化物的水溶液显碱性;Y在元素周期表中所处的周期序数与族序数相等;Z单质是将太阳能转化为电能的常用材料;W是重要的“成盐元素”,主要以钠盐的形式存在于海水中,请回答: .
.
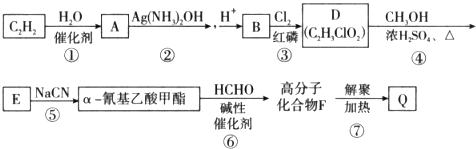
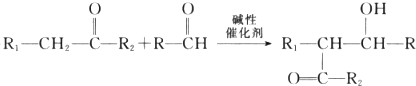
 不稳定,很快分子间脱水进行聚合,[R、R1和R2可表示氢原子、烃基、-OCH3、-CN(氰基)等基团]
不稳定,很快分子间脱水进行聚合,[R、R1和R2可表示氢原子、烃基、-OCH3、-CN(氰基)等基团] .
.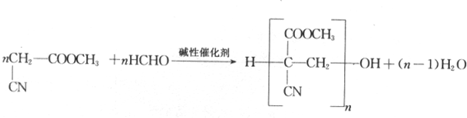 .
.
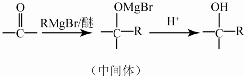
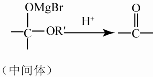
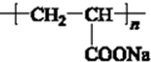

 .
.

 )外,含有的官能团名称是碳碳双键、酯基;
)外,含有的官能团名称是碳碳双键、酯基; .
.
 ,
,