题目内容
(11分)(Ⅰ)A、B、C和D代表原子序数依次增大的四种短周期元素,它们满足以下条件:
①C的原子序数是A、B的原子序数之和,A、C、D的最外层电子数和为13;
②D的原子序数是C的2倍,D的最高价氧化物对应的水化物是二元强酸。
试根据以上叙述回答:
(1)B单质的电子式为 ,画出C元素的原子结构示意图 ;
(2)下列环境问题与B与C形成的化合物有关的是 ;
A.温室效应 B.光化学烟雾 C.酸雨 D.PM2.5
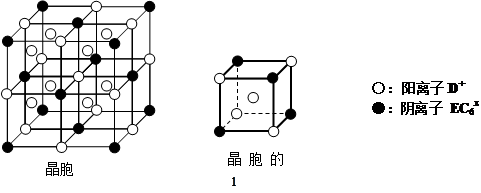
(3)A、B、C和D四种元素可形成一化合物,其原子个数之比为8∶2∶4∶1。该化合物属于 (填晶体类型)。
(Ⅱ)现有下列短周期元素相关性质的数据:
试回答下列问题:
(1)元素⑤在周期表中的位置 ;元素②的单质与CO2反应的化学方程式 ,该单质可通过电解法制得,下列金属中人类最早开发和利用的是 ;
A.铁 B.铝 C.金 D.铜
(2)元素④与元素⑦相比较,气态氢化物较稳定的是 (填结构式);
(3)元素④形成的+3和+5价的氯化物中,各原子均达到8电子稳定结构的化合物是 。(写化学式)
①C的原子序数是A、B的原子序数之和,A、C、D的最外层电子数和为13;
②D的原子序数是C的2倍,D的最高价氧化物对应的水化物是二元强酸。
试根据以上叙述回答:
(1)B单质的电子式为 ,画出C元素的原子结构示意图 ;
(2)下列环境问题与B与C形成的化合物有关的是 ;
A.温室效应 B.光化学烟雾 C.酸雨 D.PM2.5
(3)A、B、C和D四种元素可形成一化合物,其原子个数之比为8∶2∶4∶1。该化合物属于 (填晶体类型)。
(Ⅱ)现有下列短周期元素相关性质的数据:
| 元素编号 元素性质 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ |
| 原子半径(10-10m) | 0.74 | 1.60 | 1.52 | 1.10 | 0.99 | 1.86 | 0.75 |
| 最高正化合价 | | +2 | +1 | +5 | +7 | +1 | +5 |
| 最低负化合价 | -2 | | | -3 | -1 | | -3 |
(1)元素⑤在周期表中的位置 ;元素②的单质与CO2反应的化学方程式 ,该单质可通过电解法制得,下列金属中人类最早开发和利用的是 ;
A.铁 B.铝 C.金 D.铜
(2)元素④与元素⑦相比较,气态氢化物较稳定的是 (填结构式);
(3)元素④形成的+3和+5价的氯化物中,各原子均达到8电子稳定结构的化合物是 。(写化学式)
(Ⅰ)(1) (1分),
(1分),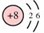 (1分);
(1分);
(2)BC (2分,有错全扣,不全扣1分);
(3)离子晶体(1分)。
(Ⅱ)(1)第三周期第ⅦA族 (1分),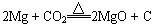 (2分,条件不写扣1分);D(1分);
(2分,条件不写扣1分);D(1分);
(2)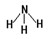 (1分);
(1分);
(3)PCl3 (1分)
 (1分),
(1分), (1分);
(1分);(2)BC (2分,有错全扣,不全扣1分);
(3)离子晶体(1分)。
(Ⅱ)(1)第三周期第ⅦA族 (1分),
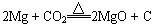 (2分,条件不写扣1分);D(1分);
(2分,条件不写扣1分);D(1分);(2)
 (1分);
(1分);(3)PCl3 (1分)
考查了元素周期律的相关知识及化学用语的书写。
(I)综合所有信息:D的最高价氧化物对应的水化物是二元强酸,可推出D为S,进而可知C为O,再由A、C、D的最外层电子数和为13可推得A为H,而C的原子序数是A、B的原子序数之和,可得B为N;
(3)物质为(NH4)2SO4,属离子化合物
(II)综合原子半径及化合价的规律可推得各元素分别为:⑤氯、④磷、⑦氮、②镁
(I)综合所有信息:D的最高价氧化物对应的水化物是二元强酸,可推出D为S,进而可知C为O,再由A、C、D的最外层电子数和为13可推得A为H,而C的原子序数是A、B的原子序数之和,可得B为N;
(3)物质为(NH4)2SO4,属离子化合物
(II)综合原子半径及化合价的规律可推得各元素分别为:⑤氯、④磷、⑦氮、②镁

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
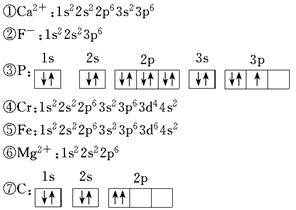
 恰好完全反应。B单质与D单质反应后可形成离子化合物
恰好完全反应。B单质与D单质反应后可形成离子化合物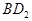 ;B单质与E单质可形成化合物BE。D的阴离子比B的阳离子多一个电子层,而E阴离子与B的阳离子电子层结构相同。
;B单质与E单质可形成化合物BE。D的阴离子比B的阳离子多一个电子层,而E阴离子与B的阳离子电子层结构相同。 的化学键类型是: .
的化学键类型是: .