题目内容
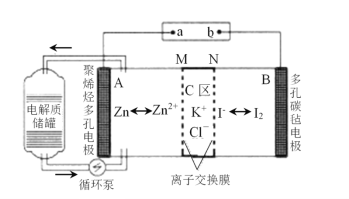
【题目】一种新型的锌碘单液流电池,其原理如下图所示。下列说法不正确的是 ( )。
A.放电时B电极反应式为:I2+2e-=2I-
B.M为阳离子交换膜,N为阴离子交换膜
C.充电时,A极增重65g时,C区增加离子数为4NA
D.放电时电解质储罐中离子总浓度增大
【答案】B
【解析】
由装置图可知,放电时,Zn是负极,负极反应式为Zn-2e-═Zn2+,石墨是正极,反应式为I2+2e-=2I-,外电路中电流由正极经过导线流向负极,充电时,阳极反应式为2I--2e-=I2、阴极反应式为Zn2++2e-=Zn,据此分析解答。
A.放电时,B电极为正极,I2得到电子生成I-,电极反应式为I2+2e-=2I-,故A正确;
B.离子交换膜是防止正负极I2、Zn接触直接发生氧化还原反应,负极区生成Zn2+、正电荷增加,正极区生成I-、负电荷增加,所以Cl-通过M膜进入负极,K+通过N膜进入正极,所以M为阴离子交换膜,N为阳离子交换膜,故B错误;
C.充电时,A极反应式Zn2++2e-=Zn,A极增重65g转移2mol电子,所以C区增加2molK+、2molCl-,离子总数为4NA,故C正确;
D.放电时,Zn是负极,负极反应式为Zn-2e-═Zn2+,石墨是正极,反应式为I2+2e-=2I-,转移2mol电子时负极生成1mol的锌离子,正极产生2mol的碘离子,所以放电时电解质储罐中离子总浓度增大,故D正确;
故答案为B。

练习册系列答案
相关题目