题目内容
12.用15.8g KMnO4与足量浓盐酸反应.反应方程式如下:2KMnO4+16HCl═2KCl+2MnCl2+5Cl2↑+8H2O 回答下列问题:(已知KMnO4的相对分子质量为158)(1)被氧化的HCl的物质的量为多少?
(2)产生的Cl2在标准状况下的体积为多少?
分析 n(KMnO4)=$\frac{15.8g}{158g/mol}$=0.1mol,结合反应2KMnO4+16HCl═2KCl+2MnCl2+5Cl2↑+8H2O及原子守恒可知,2mol氧化剂失去电子与10molHCl得到电子相同,且生成5molCl2,以此计算.
解答 解:n(KMnO4)=$\frac{15.8g}{158g/mol}$=0.1mol,
(1)设被氧化的HCl为xmol,则
2KMnO4+16HCl═2KCl+2MnCl2+5Cl2↑+8H2O~被氧化的HCl
2 10
0.1mol x
$\frac{2}{0.1mol}=\frac{10}{x}$,解得x=0.5mol,
答:被氧化的HCl的物质的量为0.5mol;
(2)由反应可知,2molKMnO4反应生成5molCl2,则0.1molKMnO4参加反应生成氯气为0.1mol×$\frac{5}{2}$=0.25mol,
产生的Cl2在标准状况下的体积为0.25mol×22.4L/mol=5.6L,
答:产生的Cl2在标准状况下的体积为5.6L.
点评 本题考查氧化还原反应的计算,为高频考点,把握氧化剂、还原剂的关系及物质的量的基本计算公式为解答的关键,侧重分析与计算能力的考查,题目难度不大.

练习册系列答案
相关题目
2.恒温下用惰性电极电解某pH=a的溶液一段时间后,测知溶液的pH没发生改变,则该电解质可能是( )
| A. | NaCl溶液 | B. | AgNO3溶液 | C. | HCl溶液 | D. | 稀Na2SO4溶液 |
3.下列关于金属腐蚀的叙述正确的是( )
| A. | 金属(M表示金属)被腐蚀的本质是:Mn++ne-=M | |
| B. | 金属不可能在碱性环境中发生电化学腐蚀 | |
| C. | 镀锌铁的镀层破损后,镀层仍能对铁起保护作用 | |
| D. | 钢管与外加直流电源的正极相连,以保护它不受腐蚀 |
20.有甲、乙、丙、丁四种金属,将它们分别投入到相同的稀盐酸中,只有丙、丁的表面有气泡产生,且丙产生的气泡比丁快;再将乙投入到甲的盐酸液中,乙的表面有甲析出.则四种金属的活动性顺序正确的是( )
| A. | 甲>乙>丙>丁 | B. | 丙>丁>乙>甲 | C. | 丙>丁>甲>乙 | D. | 无法判断 |
17.下列过程或现象中没有发生氧化还原反应的是( )
| A. | 钢铁在潮湿的环境中生锈 | |
| B. | 利用漂白粉进行自来水消毒 | |
| C. | 将FeCl3饱和溶液滴入沸水中并加热制备Fe(OH)3胶体 | |
| D. | Na2O2投入酚酞溶液中溶液先变红后褪色 |
4.某混合溶液中可能含有下列离子中的若干种:NH4+、Na+、Mg2+、Al3+、Fe2+、SO42-、NO3-、CO32-,已知各离子的浓度均约为0.1mol•L-1,现取20mL该溶液进行如下实验:
(1)向20mL该溶液张加入足量盐酸,产生的气体在空气中变为红棕色;
(2)在(1)反应后的溶液中加入过量Ba(OH)2溶液,有刺激性气味气体和有白色沉淀产生.
(3)向(2)反应的溶液中通入适量CO2,有白色沉淀甲生成.
根据上述实验情况,以下说法正确的是( )
(1)向20mL该溶液张加入足量盐酸,产生的气体在空气中变为红棕色;
(2)在(1)反应后的溶液中加入过量Ba(OH)2溶液,有刺激性气味气体和有白色沉淀产生.
(3)向(2)反应的溶液中通入适量CO2,有白色沉淀甲生成.
根据上述实验情况,以下说法正确的是( )
| A. | 该混合溶液中一定含有Fe2+、NO3-、NH4+、SO42- | |
| B. | 白色沉淀甲一定是Al(OH)3 | |
| C. | 该混合溶液中肯定含有Fe2+、NH4+、CO32-、NO3- | |
| D. | 向该混合溶液中滴加酚酞试液后呈红色 |
1.同温同压下,下列气体密度最小的是( )
| A. | N2 | B. | O2 | C. | H2S | D. | H2 |
2.下列判断正确的是( )
| A. | 离子化合物中不可能含有共价键 | |
| B. | 晶体中一定存在化学键 | |
| C. | 碱性氧化物一定是金属氧化物 | |
| D. | 直径介于1-10nm之间的微粒称为胶体 |
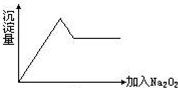 一无色透明的溶液做如下实验:
一无色透明的溶液做如下实验: