题目内容
 传统中药的砷剂俗称“砒霜”,请回答下列问题:
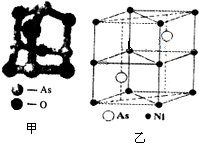
传统中药的砷剂俗称“砒霜”,请回答下列问题:(1)砷剂的分子结构如图甲所示.该化合物中As原子的杂化方式为
(2)基态砷原子的价层电子排布式为
(3)已知:
| NH3 | PH3 | AsH3 | |
| 键角/° | 107.8 | 93.6 | 91.8 |
| 熔点/℃ | -77.74 | -134 | -117 |
(4)砷酸(H3AsO4)是一种三元中强酸,根据价层电子对互斥理论推测AsO43-的空间构型为
(5)砷镍合金的晶胞如图乙所示,该晶体中与每个Ni原子距离最近的As原子有
考点:原子轨道杂化方式及杂化类型判断,原子核外电子排布,判断简单分子或离子的构型,晶胞的计算
专题:原子组成与结构专题,化学键与晶体结构
分析:(1)根据图中原子形成的共价键数判断属于哪种元素,再根据原子数写化学式;根据δ键电子对数和对孤电子对数判断As的杂化方式;
(2)主族元素基态原子的价层电子排布就是最外层电子排布;同周期电离能第ⅤA族>第ⅥA族;
(3)NH3分子间存在氢键使熔沸点升高;
(4)根据AsO43-中心原子的价层电子对数,可以推得空间类型;
(5)结合晶胞图象可知最近的共6个原子.
(2)主族元素基态原子的价层电子排布就是最外层电子排布;同周期电离能第ⅤA族>第ⅥA族;
(3)NH3分子间存在氢键使熔沸点升高;
(4)根据AsO43-中心原子的价层电子对数,可以推得空间类型;
(5)结合晶胞图象可知最近的共6个原子.
解答:
解:(1)氧原子能形成2个共价键,As形成3个共价键,由图可知分子中O原子数为6,As原子数为4,所以其化学式为As4O6;As最外层有5个电子,形成3个共价键即δ键电子对数为3,另外还有1个孤电子对,所以As的杂化方式为sp3;
故答案为:sp3;
(2)主族元素基态原子的价层电子排布就是最外层电子排布,所以基态砷原子的价层电子排布式为4s24p3,同周期电离能第ⅤA族>第ⅥA族,所以砷大于硒,故答案为:4s24p3,砷;
(3)由于NH3分子间存在氢键,熔沸点较高,故答案为:NH3分子间存在氢键使熔沸点升高;
(4)根据AsO43-中心原子的价层电子对数为
=4,所以As原子的杂化方式为sp3杂化,所以离子的空间构型为:正四面体,故答案为:正四面体;
(6)以一个顶点为中心,再结合晶胞图象可知最近的共6个原子,故答案为:6.
故答案为:sp3;
(2)主族元素基态原子的价层电子排布就是最外层电子排布,所以基态砷原子的价层电子排布式为4s24p3,同周期电离能第ⅤA族>第ⅥA族,所以砷大于硒,故答案为:4s24p3,砷;
(3)由于NH3分子间存在氢键,熔沸点较高,故答案为:NH3分子间存在氢键使熔沸点升高;
(4)根据AsO43-中心原子的价层电子对数为
| 5+3 |
| 2 |
(6)以一个顶点为中心,再结合晶胞图象可知最近的共6个原子,故答案为:6.
点评:本题考查较为综合,涉及元素周期律的递变规律、杂化类型的判断、电子排布式以及氢键等知识,题目难度较大,本题的易错点为晶胞的有关计算,注意有关知识的积累.

练习册系列答案
相关题目
下列各组物质在不同条件下反应时,均能得到不同产物,其中主要是由于反应物的浓度不同而引起的是( )
| A、Fe+H2SO4 |
| B、Cu+HNO3 |
| C、NaOH+CO2 |
| D、AlCl3+NaOH |
在100mL某混合酸中,c(HNO3)=0.4mol?L-1,c(H2SO4)=0.1mol?L-1,向其中加入1.92g铜粉,待充分反应后,忽略溶液体积的变化,溶液中Cu2+的物质的量浓度为( )
| A、0.15 mol?L-1 |
| B、0.30 mol?L-1 |
| C、0.225 mol?L-1 |
| D、无法计算 |
下列生产实践中不宜用熟石灰的是( )
| A、建筑工业上制三合土 |
| B、降低土壤的酸性,改良土壤 |
| C、处理呈酸性的工业废水 |
| D、干燥气体 |
下列关于有机物的说法中不正确的是( )
| A、乙醇和乙酸均可以使酸性高锰酸钾溶液褪色 |
| B、淀粉、油脂、蛋白质在一定条件下都能发生水解反应 |
| C、正丁烷比异丁烷的沸点高 |
| D、乙醇和乙酸均能与金属钠能反应 |

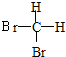 和
和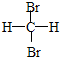 E.CH4和CH3(CH2)2CH3
E.CH4和CH3(CH2)2CH3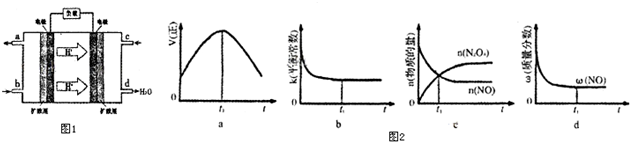
 某同学欲探究Cl2、Br2、I2之间的变化:
某同学欲探究Cl2、Br2、I2之间的变化: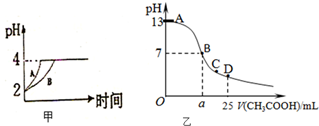 化学学科中的平衡理论主要包括:化学平衡、电离平衡、水解平衡和溶解平衡四种,且均符合勒夏特列原理.请回答下列问题:
化学学科中的平衡理论主要包括:化学平衡、电离平衡、水解平衡和溶解平衡四种,且均符合勒夏特列原理.请回答下列问题: