题目内容
在100mL某混合酸中,c(HNO3)=0.4mol?L-1,c(H2SO4)=0.1mol?L-1,向其中加入1.92g铜粉,待充分反应后,忽略溶液体积的变化,溶液中Cu2+的物质的量浓度为( )
| A、0.15 mol?L-1 |
| B、0.30 mol?L-1 |
| C、0.225 mol?L-1 |
| D、无法计算 |
考点:物质的量浓度的相关计算
专题:物质的量浓度和溶解度专题
分析:100mL混合液中显示的物质的量为:n(HNO3)=0.1L×0.4mol/L=0.04mol,含有硫酸的物质的量为:n(H2SO4)=0.1L×0.1moL/L=0.01moL,溶液中氢离子浓度为:n(H+)=0.04moL+2×0.01moL=0.06mol,1.92g铜的物质的量为:n(Cu)=
=0.03mol,根据反应:3Cu+2NO3-+8H+=3Cu2++2NO+4H2O判断过量情况,根据不足量进行计算即可.
| 1.92g |
| 64g/mol |
解答:
解:100mL该混合液中含有的硝酸、硫酸的物质的量分别为:n(HNO3)=0.1L×0.4mol/L=0.04mol,n(H2SO4)=0.1L×0.1moL/L=0.01moL,则含有氢离子的总物质的量为:n(H+)=0.04moL+2×0.01moL=0.06mol,
1.92g铜的物质的量为:n(Cu)=
=0.03mol,
铜与硝酸发生的反应为:3Cu+2NO3-+8H+=3Cu2++2NO+4H2O
3mol 2mol 8mol
0.03mol 0.04mol 0.08mol
根据反应关系可以看出,氢离子不足,Cu过量,反应生成的铜离子小于按照氢离子浓度计算,
则生成的铜离子的物质的量为:n(Cu2+)=
×n(H+)=0.06mol×
=0.0225mol,
溶液中Cu2+的物质的量浓度为:c(Cu2+)=
=0.225mol/L,
故选C.
1.92g铜的物质的量为:n(Cu)=
| 1.92g |
| 64g/mol |
铜与硝酸发生的反应为:3Cu+2NO3-+8H+=3Cu2++2NO+4H2O
3mol 2mol 8mol
0.03mol 0.04mol 0.08mol
根据反应关系可以看出,氢离子不足,Cu过量,反应生成的铜离子小于按照氢离子浓度计算,
则生成的铜离子的物质的量为:n(Cu2+)=
| 3 |
| 8 |
| 3 |
| 8 |
溶液中Cu2+的物质的量浓度为:c(Cu2+)=
| 0.0225mol |
| 0.1L |
故选C.
点评:本题考查物质的量浓度的计算,题目难度中等,解答该题的关键是把握反应的离子方程式,根据离子方程式判断反应物的过量情况.

练习册系列答案
 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案
相关题目
常温下,下列溶液中可能大量共存的离子组是( )
| A、水电离产生的c(H+)=1×10-12mol/L的溶液中:AlO2-、S2-、PO43-、Na+ |
| B、加入金属镁能产生H2的溶液中:Na+、HCO3-、SO42-、Al3+ |
| C、能使Al溶解产生H2的溶液中:NH4+、Na+、SiO32-、CO32- |
| D、含有大量Fe2+的溶液中:K+、Mg2+、ClO-、SO42- |
既可以使溴水褪色,又可以使酸性高锰酸钾溶液褪色的气体有( )
| A、CH4 |
| B、CO2 |
| C、C2H4 |
| D、C2H6 |
下列有关实验现象的描述,正确的是( )
| A、在盛有苯的试管中加入几滴酸性KMnO4溶液,可观察到紫色褪去 |
| B、向鸡蛋清溶液中滴加饱和CuSO4溶液,有固体析出,再加入足量蒸馏水,固体可以重新溶解 |
| C、用灯光照射盛有CH4与Cl2(体积比1:4)的集气瓶后,可观察到瓶内壁附有液态物质 |
| D、将红热的铜丝迅速插入乙醇中,可观察到铜丝表面变黑,反复多次,并能闻到香味 |
下列情况下,一定能在溶液中同时大量共存的离子组是( )
| A、pH=2的溶液中:SO42-、K+、NO3-、Mg2+ |
| B、pH试纸呈现红色的溶液:Fe2+、K+、NO3-、Na+ |
| C、水电离出的c(H+)=10-12mol/L的溶液中:Na+、HCO3-、Cl-、SO42- |
| D、中性溶液中:Fe3+、Al3+、NO3-、I-、Cl- |
绿色化学的核心内涵是在反应过程中和化工生产中,尽量减少或彻底消除使用和产生有害物质,下列说法不正确的是( )
| A、大量使用天然气作燃料对环境无任何污染 |
| B、制硫酸工厂的尾气常用碱液吸收 |
| C、氢气是一种无污染能源 |
| D、为消除制硫酸尾气中二氧化硫的污染,可杂燃烧炉中加入石灰石固硫 |

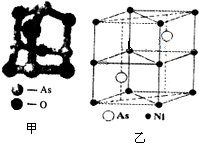 传统中药的砷剂俗称“砒霜”,请回答下列问题:
传统中药的砷剂俗称“砒霜”,请回答下列问题: