题目内容
下列关于甲、乙、丙、丁四个图象的说法中,正确的是( )
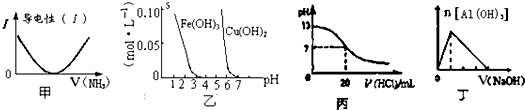

| A、图甲表示向乙酸溶液中通入NH3过程中溶液导电性的变化 |
| B、由图乙可知若除去CuSO4溶液中的Fe3+可采用向溶液中加入适量CuO至pH在4左右 |
| C、图丙表示25°C时,用0.1mol/L盐酸滴定20mL 0.1mol.L-1氨水,溶液的pH随加入盐酸体积的变化 |
| D、图丁表示向Al2(SO4)3溶液中滴入NaOH溶液,生成Al(OH)3沉淀的量随NaOH溶液体积的变化 |
考点:酸碱混合时的定性判断及有关ph的计算,电解质溶液的导电性,难溶电解质的溶解平衡及沉淀转化的本质,镁、铝的重要化合物
专题:图示题
分析:A.向乙酸溶液中通入NH3生成乙酸铵,溶液导电性增强;
B.加入适量CuO至pH在4左右,可使铁离子生成氢氧化铁沉淀而除去;
C.一水合氨为弱碱,不能完全电离;
D.生成沉淀和沉淀溶解消耗氢氧化钠的比值为3:1.
B.加入适量CuO至pH在4左右,可使铁离子生成氢氧化铁沉淀而除去;
C.一水合氨为弱碱,不能完全电离;
D.生成沉淀和沉淀溶解消耗氢氧化钠的比值为3:1.
解答:
解:A.乙酸和一水合氨都是弱电解质,向乙酸溶液中通入NH3生成乙酸铵,溶液导电性增强,故A错误;
B.由图象可知,加入适量CuO至pH在4左右,可使铁离子生成氢氧化铁沉淀而除去,故B正确;
C.一水合氨为弱碱,不能完全电离,0.1mol.L-1氨水的pH<13,故C错误;
D.生成沉淀和沉淀溶解消耗氢氧化钠的比值为3:1,图象为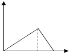 ,故D错误.
,故D错误.
故选B.
B.由图象可知,加入适量CuO至pH在4左右,可使铁离子生成氢氧化铁沉淀而除去,故B正确;
C.一水合氨为弱碱,不能完全电离,0.1mol.L-1氨水的pH<13,故C错误;
D.生成沉淀和沉淀溶解消耗氢氧化钠的比值为3:1,图象为
 ,故D错误.
,故D错误.故选B.
点评:本题考查较为综合,涉及反应热与焓变、弱电解质的电离、难溶电解质的溶解平衡以及氢氧化铝的性质,为高考常见题型,侧重于考查学生化学知识的综合运用能力,题目难度中等.

练习册系列答案
相关题目
在通常条件下,下列各组物质的性质排列正确的是( )
| A、水溶性:NH3>H2S>I2 |
| B、沸点:HF>HCl>HBr |
| C、硬度:金刚石>晶体硅>碳化硅 |
| D、熔点:LiF>KF>NaF |
要除去FeCl2中含有的Fe3+、Cu2+、H+,应选择的试剂是( )
| A、氯气 | B、NaOH |
| C、铁粉 | D、氨水 |
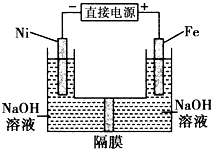 高铁酸盐在能源环保领域有广泛用途.用镍(Ni)、铁做电极电解浓NaOH溶液制备高铁酸盐Na2FeO4的装置如图所示.下列推断合理的是( )
高铁酸盐在能源环保领域有广泛用途.用镍(Ni)、铁做电极电解浓NaOH溶液制备高铁酸盐Na2FeO4的装置如图所示.下列推断合理的是( )| A、铁是阳极,电极反应为Fe-6e-+4H2O═FeO42-+8H+ |
| B、镍电极上的电极反应为2H2O+2e-═H2↑+2OH- |
| C、若隔膜为阴离子交换膜,则OH-自右向左移动 |
| D、电解时阳极区pH降低、阴极区pH升高,最终溶液pH不变 |
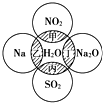 图中两圆圈相交的阴影部分表示圆圈内物质相互发生的反应,其中属于氧化还原反应,但水既不作氧化剂也不作还原剂的是( )
图中两圆圈相交的阴影部分表示圆圈内物质相互发生的反应,其中属于氧化还原反应,但水既不作氧化剂也不作还原剂的是( )