题目内容
【题目】高铁酸盐是优良的多功能水处理剂。某实验小组采用如图装置制备高铁酸钾![]() 并探究其性质用途。
并探究其性质用途。
资料:![]() 为紫色固体,微溶于KOH溶液,难溶于有机溶剂;具有强氧化性,在酸性或中性溶液中紫色快速褪去并产生
为紫色固体,微溶于KOH溶液,难溶于有机溶剂;具有强氧化性,在酸性或中性溶液中紫色快速褪去并产生![]() ,在碱性溶液中较稳定。
,在碱性溶液中较稳定。
Ⅰ![]() 制备
制备![]() 夹持、加热等装置略
夹持、加热等装置略![]()
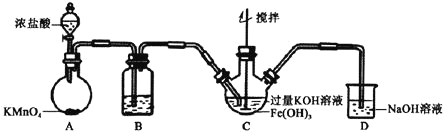
(1)![]() 中发生反应的化学方程式为________________;B中所用试剂为________________。
中发生反应的化学方程式为________________;B中所用试剂为________________。
(2)C中反应为放热反应,而反应温度须控制在![]() ,可使用的控温方法为________,充分反应后得到紫色固体,反应方程式为________________________。反应中KOH必须过量的原因是________________________。
,可使用的控温方法为________,充分反应后得到紫色固体,反应方程式为________________________。反应中KOH必须过量的原因是________________________。
(3)C中混合物经过滤、洗涤、干燥,得纯净高铁酸钾晶体,洗涤时洗涤剂可选用________。
![]() 冰水
冰水 ![]() 溶液
溶液 ![]() 异丙醇
异丙醇
Ⅱ![]() 探究
探究![]() 的性质
的性质
(4)![]() 可以将废水中的
可以将废水中的![]() 氧化为
氧化为![]() ,实验表明,
,实验表明,![]() 时
时![]() 去除效果最佳。配平反应离子方程式:______FeO42-+___________CN-__________H2O→Fe(OH)3↓+_______CNO-_________OH-。_________
去除效果最佳。配平反应离子方程式:______FeO42-+___________CN-__________H2O→Fe(OH)3↓+_______CNO-_________OH-。_________
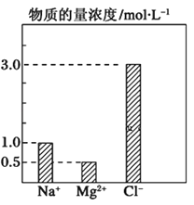
现处理含![]() 离子浓度为
离子浓度为![]() 的废水
的废水![]() ,至少需要
,至少需要![]() ________g。
________g。
(5)用滴定分析法测定样品中![]() 的纯度:现称取
的纯度:现称取![]() 制备的样品溶于适量氢氧化钾溶液中,加入稍过量的
制备的样品溶于适量氢氧化钾溶液中,加入稍过量的![]() ,充分反应后过滤,滤液定容于250mL容量瓶中。
,充分反应后过滤,滤液定容于250mL容量瓶中。
每次取![]() 加入稀硫酸酸化,用
加入稀硫酸酸化,用![]() 的
的![]() 标准溶液滴定,三次滴定消耗标准溶液的平均体积为
标准溶液滴定,三次滴定消耗标准溶液的平均体积为![]() 。有关反应的离子方程式为:
。有关反应的离子方程式为:
![]() ;
;
![]() ;
;
![]() 。
。
样品中高铁酸钾的质量分数为________________。
【答案】![]() 饱和食盐水 冰水浴或冷水浴
饱和食盐水 冰水浴或冷水浴 ![]() 保持溶液碱性,防止
保持溶液碱性,防止![]() 变质 c
变质 c ![]() ; 3 ; 5 ; 2 ; 3 ; 4 66
; 3 ; 5 ; 2 ; 3 ; 4 66 ![]()
【解析】
![]() 中高锰酸钾与浓盐酸发生反应生成氯化钾、氯化锰、氯气和水;A中生成氯气含有杂质氯化氢;
中高锰酸钾与浓盐酸发生反应生成氯化钾、氯化锰、氯气和水;A中生成氯气含有杂质氯化氢;
![]() 反应温度须控制在
反应温度须控制在![]() ,可使用的控温方法为冰水浴或冷水浴;
,可使用的控温方法为冰水浴或冷水浴;![]() 在碱性溶液中稳定;
在碱性溶液中稳定;
![]() 根据
根据![]() 难溶于有机溶剂选择洗涤剂;
难溶于有机溶剂选择洗涤剂;
Ⅱ![]() 元素的化合价由
元素的化合价由![]() 价降低为
价降低为![]() 价,C元素的化合价由
价,C元素的化合价由![]() 价升高为
价升高为![]() 价,由电子、电荷及原子守恒配平离子方程式;根据反应离子方程式计算需要
价,由电子、电荷及原子守恒配平离子方程式;根据反应离子方程式计算需要![]() 的质量;
的质量;
![]() 根据反应
根据反应![]() 建立关系式
建立关系式![]() ,根据关系式计算样品纯度。
,根据关系式计算样品纯度。
Ⅰ![]() 中为高锰酸钾与浓盐酸发生反应,相应的化学方程式为
中为高锰酸钾与浓盐酸发生反应,相应的化学方程式为![]() ;A中生成氯气含有杂质氯化氢,B中所用试剂为饱和食盐水以除去氯气中的氯化氢气体;
;A中生成氯气含有杂质氯化氢,B中所用试剂为饱和食盐水以除去氯气中的氯化氢气体;
![]() 中反应为放热反应,而反应温度须控制在
中反应为放热反应,而反应温度须控制在![]() ,可使用的控温方法为冰水浴或冷水浴,充分反应后得到紫色固体,反应方程式为
,可使用的控温方法为冰水浴或冷水浴,充分反应后得到紫色固体,反应方程式为![]() ,
,![]() 在碱性溶液中稳定,所以反应中KOH必须过量,防止
在碱性溶液中稳定,所以反应中KOH必须过量,防止![]() 变质;
变质;
![]() 中混合物经过滤、洗涤、干燥,得纯浄高铁酸钾晶体,根据
中混合物经过滤、洗涤、干燥,得纯浄高铁酸钾晶体,根据![]() 难溶于有机溶剂,所以洗涤剂可选用异丙醇,选C;
难溶于有机溶剂,所以洗涤剂可选用异丙醇,选C;
Ⅱ![]() 元素的化合价由
元素的化合价由![]() 价降低为
价降低为![]() 价,C元素的化合价由
价,C元素的化合价由![]() 价升高为
价升高为![]() 价,由电子、电荷及原子守恒可知离子反应为
价,由电子、电荷及原子守恒可知离子反应为![]() ;根据反应离子方程式可知处理含
;根据反应离子方程式可知处理含![]() 离子浓度为
离子浓度为![]() 的废水
的废水![]() ,至少需要
,至少需要![]() 为
为![]() ;
;
![]() 根据反应
根据反应![]() 可知:
可知:![]() ,
,
1 mol 3mol
n ![]()
则![]() ,所以样品中高铁酸钾的质量分数为
,所以样品中高铁酸钾的质量分数为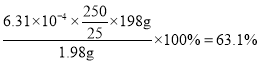 。
。

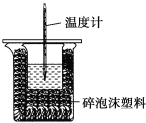
【题目】某实验小组用100mL0.50mol/LNaOH溶液与60mL0.50mol/L硫酸进行中和热的测定。装置如图所示,回答下列问题:
(1)若实验共需要400mLNaOH溶液,实验室在配制该溶液时,则需要称量NaOH固体____g。
(2)图中装置缺少的仪器是____。
(3)硫酸稍过量的原因是____。
(4)请填写下表中的平均温度差:
实验 次数 | 起始温度T1/℃ | 终止温度 T2/℃ | 平均温度差 (T2-T1)/℃ | ||
HCl | NaOH | 平均值 | |||
1 | 26.2 | 26.0 | 26.1 | 30.1 | ____ |
2 | 27.0 | 27.4 | 27.2 | 33.3 | |
3 | 25.9 | 25.9 | 25.9 | 29.8 | |
4 | 26.4 | 26.2 | 26.3 | 30.4 | |
(5)近似认为0.50 mol/L NaOH溶液与0.50 mol/L硫酸溶液的密度都是1 g/cm3,中和后生成溶液的比热容为c=4.18J/(g℃)则上述实验中和热ΔH=___(取小数点后一位)
(6)上述实验结果与57.3kJ/mol有偏差产生偏差的原因可能是____
A.量取NaOH溶液时仰视读数
B.为了使反应充分,可以向酸中分次加入碱
C.实验装置保温隔热效果差
D.用铜丝代替玻璃棒搅拌
【题目】在2L密闭容器内,800℃时反应2NO(g)+O2(g)→2NO2(g)体系中,n(NO)随时间的变化如下表:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)上述反应_____(填“是”或“不是”)可逆反应,在第5s时,NO的转化率为____。
(2)如图所示,表示NO2变化曲线的是____。用O2表示0~2s内该反应的平均速率v=____。
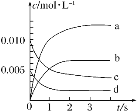
(3)能说明该反应已达到平衡状态的是____(填字母)。
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v逆(NO)=2v正(O2) d.容器内密度保持不变